
Wetenschap
Waarom wordt chemische verandering omgekeerd?
chemische veranderingen die kunnen worden omgekeerd
* Omkeerbare reacties: Sommige chemische reacties kunnen in beide richtingen doorgaan, wat betekent dat de producten kunnen reageren om de oorspronkelijke reactanten te vormen. Dit wordt vaak aangegeven door een dubbele pijl (⇌).
* Voorbeeld: De vorming van ammoniak uit stikstof en waterstof is omkeerbaar:
N₂ + 3H₂ ⇌ 2NH₃
* Fysieke veranderingen: Veel veranderingen die we als chemische stof beschouwen, zijn eigenlijk fysieke veranderingen die kunnen worden omgekeerd. Deze omvatten veranderingen in staat of vorm, niet de samenstelling van de stof.
* Voorbeeld: Smeltend ijs (vast water) in vloeibaar water is omkeerbaar door het weer in ijs te bevriezen.
chemische veranderingen die moeilijk of onmogelijk te omzeilen zijn
* onomkeerbare reacties: Sommige reacties zijn onomkeerbaar, wat betekent dat de producten niet gemakkelijk kunnen reageren om de oorspronkelijke reactanten te vormen. Deze omvatten vaak:
* Vorming van een gas: Burning Wood geeft koolstofdioxide vrij, dat niet gemakkelijk recombineert met de resterende as.
* Vorming van een neerslag: Het mengen van oplossingen van loodnitraat- en kaliumjodide vormen lood jodide -neerslag. Hoewel het mogelijk is om het neerslag te scheiden, is het niet hetzelfde als het omkeren van de chemische reactie.
* Ontledingsreacties: Het afbreken van grote moleculen in kleinere kan moeilijk zijn om terug te keren (bijv. Brandende brandstof).
factoren die de omkeerbaarheid beïnvloeden
* energie: Chemische reacties die veel energie vrijgeven (exotherme) zijn over het algemeen moeilijker te keren dan die welke energie absorberen (endotherm).
* Entropie: Reacties die de wanorde (entropie) verhogen, zijn moeilijker om te keren dan die die de stoornis verminderen.
* voorwaarden: Temperatuur, druk en katalysatoren kunnen de omkeerbaarheid van een reactie beïnvloeden.
Sleutelpunt: Of een chemische verandering kan worden omgekeerd, hangt af van de specifieke betrokken reactie en de omstandigheden waaronder deze zich voordoet.
 Een mechanisme voor het ontwerpen van legeringen met hoge entropie met verbeterde magnetische eigenschappen
Een mechanisme voor het ontwerpen van legeringen met hoge entropie met verbeterde magnetische eigenschappen Over vloeibare zuurstof
Over vloeibare zuurstof  Zijde kan de gevoeligheid verbeteren, flexibiliteit van draagbare lichaamssensoren
Zijde kan de gevoeligheid verbeteren, flexibiliteit van draagbare lichaamssensoren Hoe helpt de koeltoren van nucleaire reactie de thermische vervuiling van Lissen?
Hoe helpt de koeltoren van nucleaire reactie de thermische vervuiling van Lissen?  Bevatten stoom en water hetzelfde chemische materiaal?
Bevatten stoom en water hetzelfde chemische materiaal?
 De ontbrekende schakel tussen exploderende sterren, wolken, en klimaat op aarde
De ontbrekende schakel tussen exploderende sterren, wolken, en klimaat op aarde Regelmatig affakkelen op TRAPPIST-1 – niet geschikt voor bewoonbaarheid?
Regelmatig affakkelen op TRAPPIST-1 – niet geschikt voor bewoonbaarheid?  Satelliet ziet de vorming van tropische depressie in de oostelijke Stille Oceaan 13E
Satelliet ziet de vorming van tropische depressie in de oostelijke Stille Oceaan 13E Aqua Satellite zoomt in op het kleine oog van Super Typhoon Maria
Aqua Satellite zoomt in op het kleine oog van Super Typhoon Maria Wat is een frisse waterlichaam dat volledig omringd is door het land?
Wat is een frisse waterlichaam dat volledig omringd is door het land?
Hoofdlijnen
- Wanneer ß-32 P-ATP wordt geïncubeerd in een eukaryotisch celextract dat in staat is om transcriptie en RNA-verwerking in staat te zijn, verschijnt het label M-RNA?
- Schedelscans vertellen het verhaal van hoe 's werelds eerste honden hun prooi vingen
- Hoe virussen werken
- Proteolytisch enzym uitgescheiden als pro-eenzym in het gi-kanaal--waarom?
- Wat is de term van emulgering in de biologie?
- Hoe nemen we beslissingen?
- Wat zijn de opslagkamers binnen de cel?
- Geheime taal van cellen? Nieuwe celberekeningen ontdekt
- Waar is het proces van het maken van RNA van DNA in cel?
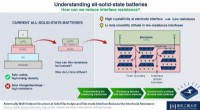
- Glashelder maken:kristalliniteit vermindert de weerstand in volledig solid-state batterijen
- Nieuwe methode van warmtegeleiding kan een game changer zijn voor serverparken en vliegtuigen

- Door polyurethaan afbreekbaar te maken, krijgen de componenten een tweede leven

- Licht en peptiden:nieuwe methode diversifieert natuurlijke bouwstenen van het leven

- Wetenschappers ontdekken bindend geheim achter eiwitsuperlijm
 Soorten metaalverhardingsprocessen
Soorten metaalverhardingsprocessen  Is de engel van breking afhankelijk van de golflengte?
Is de engel van breking afhankelijk van de golflengte?  Natuurkundigen leggen de eerste geluiden vast van hitte die in een supervloeistof klotst, en onthullen hoe hitte zich als een golf kan voortbewegen
Natuurkundigen leggen de eerste geluiden vast van hitte die in een supervloeistof klotst, en onthullen hoe hitte zich als een golf kan voortbewegen  Onderzoek ondersteunt de zorgen van demonstranten over de toekomst van Llobregat Delta
Onderzoek ondersteunt de zorgen van demonstranten over de toekomst van Llobregat Delta Waarom is diamant de moeilijkste stof?
Waarom is diamant de moeilijkste stof?  Bomen kunnen boerderijen duurzamer maken. Hier leest u hoe u boeren kunt helpen met planten
Bomen kunnen boerderijen duurzamer maken. Hier leest u hoe u boeren kunt helpen met planten  Sluit Elon Musk een lastig Twitter-account of is hij aan het plagen? (Update)
Sluit Elon Musk een lastig Twitter-account of is hij aan het plagen? (Update)  Actieve werkplekken op kantoor
Actieve werkplekken op kantoor
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

