
Wetenschap
Waarom is diamant de moeilijkste stof?
1. Sterke covalente bindingen:
* Diamond's atomen zijn gerangschikt in een tetraëdrisch rooster. Elk koolstofatoom vormt vier sterke covalente bindingen met zijn aangrenzende koolstofatomen.
* Deze bindingen zijn extreem sterk en vereisen een aanzienlijke hoeveelheid energie om te breken. Dit geeft Diamond zijn hoge hardheid en weerstand tegen krassen.
2. Strak gepakte structuur:
* De tetraëdrische opstelling van koolstofatomen in diamant creëert een strak gepakte, starre structuur.
* Deze structuur minimaliseert de ruimte tussen atomen, waardoor het extreem moeilijk is om te vervormen.
3. Hoog smeltpunt:
* De sterke covalente bindingen in diamant vereisen een hoge temperatuur om te breken. Dit vertaalt zich in een zeer hoog smeltpunt, wat verder bijdraagt aan zijn hardheid.
4. Afwezigheid van splitsingsvlakken:
* In tegenstelling tot veel andere mineralen heeft Diamond geen verschillende splitsingvlakken. Splitsingvlakken zijn zwakke gebieden waar een mineraal gemakkelijk kan breken.
* De afwezigheid van deze vlakken in diamant maakt het moeilijk om te breken.
Andere factoren:
* de hardheid van Diamond wordt ook beïnvloed door factoren zoals zuiverheid en kristallijne structuur. Perfect pure en goed gekristalliseerde diamanten zijn het moeilijkst.
Belangrijke opmerking:
Hoewel Diamond de moeilijkste natuurlijk voorkomende substantie is, zijn sommige synthetische materialen, zoals kubieke boornitride (CBN), nog moeilijker. Diamant blijft echter het moeilijkst gevonden mineraal.
 Waarom is chromatografie een fysiek proces?
Waarom is chromatografie een fysiek proces?  Welke chemische stof is LoI?
Welke chemische stof is LoI?  Team haalt inspiratie uit natuurlijke wonderen om nieuwe materialen te maken
Team haalt inspiratie uit natuurlijke wonderen om nieuwe materialen te maken Hoe kunt u het effect van de temperatuur op de chemische reactie van de snelheid tussen bakpoeder en azijn bepalen?
Hoe kunt u het effect van de temperatuur op de chemische reactie van de snelheid tussen bakpoeder en azijn bepalen?  Wat is een mengsel waarin monsters niet noodzakelijkerwijs bestaan uit exact dezelfde proporties?
Wat is een mengsel waarin monsters niet noodzakelijkerwijs bestaan uit exact dezelfde proporties?
 NASA ziet tropische cycloon Olga samensmelten met een koufront
NASA ziet tropische cycloon Olga samensmelten met een koufront Verandering van ag op lange termijn heeft invloed op de waterkwaliteit van de beek
Verandering van ag op lange termijn heeft invloed op de waterkwaliteit van de beek Black Saturday-bosbranden:hebben we een gebrekkig systeem gerepareerd?
Black Saturday-bosbranden:hebben we een gebrekkig systeem gerepareerd? EU-hof verwerpt klimaatzaak historische burgers
EU-hof verwerpt klimaatzaak historische burgers Een Europese studie onderzoekt hoe de landbouw rivieren beïnvloedt
Een Europese studie onderzoekt hoe de landbouw rivieren beïnvloedt
Hoofdlijnen
- Is apterous vleugels seks gekoppeld in fruitvliegen?
- Tand snel, tand nieuwsgierig? Nieuwe studie onthult een nieuwe benadering van plantaardig dieet en unieke dinosaurussen met lange nek
- Tijdens de meiose resulteert het proces van oversteken in nieuwe combinaties van allelen omdat?
- Welke ziekte omvat de afbraak van luchtzakken?
- Zich in het volle zicht verbergen - Ontdekking roept vragen op over de schaal van de over het hoofd geziene biodiversiteit
- Hoe beïnvloedt hypothese een wetenschappelijk onderzoek?
- Voorspelling (biologie): definitie, soorten en voorbeelden
- Wat zat er achter het aardappeltekort in Australië? Nat weer en moeilijk te beheersen ziekten
- Hoe dodelijke parasieten ervoor kiezen mannelijk te zijn:Onderzoekers onthullen genexpressie gedurende de levenscyclus van Cryptosporidium
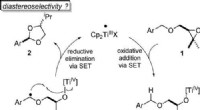
- Houd het simpel:het synthetiseren van nuttige organische verbindingen is nu gemakkelijker en goedkoper gemaakt

- Bio-ingenieurs onthullen verrassende zintuiglijke en zelfgenezende vermogens van zeedieren

- Onderzoekers ontwikkelen duurzaam katalyseproces
- Wetenschappers zetten giftige pesticiden om in behandeling tegen antibioticaresistente bacteriën
- Video:Waarom plastic flessen worden gerecycled tot kleding

 De lessen delen die zijn geleerd tijdens de overstroming van Colorado in 2013
De lessen delen die zijn geleerd tijdens de overstroming van Colorado in 2013 Elektrische auto's:speciale kleurstoffen kunnen onnodige motorvervangingen voorkomen
Elektrische auto's:speciale kleurstoffen kunnen onnodige motorvervangingen voorkomen Wetenschappers lanceren zoektocht om kwantumsensoren te ontwikkelen voor het onderzoeken van kwantummaterialen
Wetenschappers lanceren zoektocht om kwantumsensoren te ontwikkelen voor het onderzoeken van kwantummaterialen Een spuit piping maken
Een spuit piping maken Basiswiskunde leren voor volwassenen
Basiswiskunde leren voor volwassenen Wat zijn maanhooglanden?
Wat zijn maanhooglanden?  Wat is het meest radioactieve element in het universum en wat zijn de eigenschappen ervan die het zo radioactief maken?
Wat is het meest radioactieve element in het universum en wat zijn de eigenschappen ervan die het zo radioactief maken?  De mystieke betekenis van nummer 727
De mystieke betekenis van nummer 727
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

