
Wetenschap
Coëfficiënten voor zwavelzuur plus aluminiumhydroxide - sulfietwater?
Onevenwichtige vergelijking:
H₂so₃ + Al (OH) ₃ → Al₂ (So₃) ₃ + H₂o
het balanceren van de vergelijking:
1. Balans aluminium (AL): Er zijn 2 AL -atomen aan de productzijde en 1 aan de reactantzijde. Voeg een coëfficiënt van 2 toe voor AL (OH) ₃:
H₂so₃ + 2 AL (OH) ₃ → Al₂ (So₃) ₃ + H₂o
2. Balans van zwavel (s): Er zijn 3 s atomen aan de productzijde en 1 aan de reactantzijde. Voeg een coëfficiënt van 3 toe voor h₂so₃:
3 H₂so₃ + 2 AL (OH) ₃ → Al₂ (So₃) ₃ + H₂o
3. Balans zuurstof (O): Er zijn 12 O -atomen aan de productzijde en 12 aan de reactantzijde.
4. Balans waterstof (H): Er zijn 12 uur atomen aan de reactantzijde en 2 aan de productzijde. Voeg een coëfficiënt van 6 toe voor h₂o:
3 H₂so₃ + 2 AL (OH) ₃ → Al₂ (So₃) ₃ + 6 H₂o
Balanced vergelijking:
3 H₂SO₃ + 2 AL (OH) ₃ → Al₂ (So₃) ₃ + 6 H₂o
coëfficiënten:
* h₂so₃: 3
* al (oh) ₃: 2
* al₂ (So₃) ₃: 1
* h₂o: 6
 Vastestofreactie tussen meerfasige keramiek met meerdere componenten verbetert de ablatieprestaties, zo blijkt uit onderzoek
Vastestofreactie tussen meerfasige keramiek met meerdere componenten verbetert de ablatieprestaties, zo blijkt uit onderzoek  Olievlekken behandelen met chemische dispergeermiddelen:is het middel erger dan de kwaal?
Olievlekken behandelen met chemische dispergeermiddelen:is het middel erger dan de kwaal?  Wat is de evenwichtige vergelijking voor berylliumcarbonaat salpeterzuur?
Wat is de evenwichtige vergelijking voor berylliumcarbonaat salpeterzuur?  Sneller en groener zuiveringsproces met kooldioxide
Sneller en groener zuiveringsproces met kooldioxide Gehyperpolariseerde proton-MRI gebruikt om metabolische processen in realtime te observeren
Gehyperpolariseerde proton-MRI gebruikt om metabolische processen in realtime te observeren
Hoofdlijnen
- Wat is de eerste barrière voor genenstroom in allopatrische speciatie?
- Hoe een ‘evolutionaire speeltuin’ plantengenen bij elkaar brengt
- Your Body On: A Horror Movie
- Waar zou je naar kunnen zoeken in een Coleus -blad om te bepalen of fotosynthese zich voordoet?
- Hoe heet Red Butterfly?
- Onderzoekers gebruiken kunstmatige membranen om te laten zien hoe een bepaald eiwit de mitochondriën bereikt
- Welk element is aanwezig in een fosfolipide en niet in chitine?
- Meer bewijs dat Neanderthalers niet dom waren:ze maakten hun eigen touwtje
- Twee soorten variabele in de wetenschap?
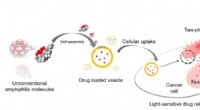
- Nieuwe technologie voor de levering van geneesmiddelen tegen kanker op aanvraag
- De rol van hydrofobe moleculen in katalytische reacties

- Onderzoekers boeken vooruitgang in ontziltingstechnologie

- Onderzoekers boeken vooruitgang in de controle over kameleonachtig materiaal voor computers van de volgende generatie

- Massaspectrometrische beeldvormingstechniek maakt diagnose eenvoudiger en slimmer

 Lava stroomt uit krater terwijl de Indonesische berg Merapi uitbarst
Lava stroomt uit krater terwijl de Indonesische berg Merapi uitbarst Door de koolstofemissies van veengebieden te meten, kan de klimaatimpact van ontwikkeling worden gemeten
Door de koolstofemissies van veengebieden te meten, kan de klimaatimpact van ontwikkeling worden gemeten Hoe de pandemie scheuren in wereldwijde toeleveringsketens aan het licht bracht
Hoe de pandemie scheuren in wereldwijde toeleveringsketens aan het licht bracht Wat is een hulpmiddel dat energie overbrengt?
Wat is een hulpmiddel dat energie overbrengt?  Wat is de belangrijkste functie van de hersenen?
Wat is de belangrijkste functie van de hersenen?  NASA krijgt tropische storm Leslie bij de staart
NASA krijgt tropische storm Leslie bij de staart Fossielen tonen aan dat er vóór de dinosauriërs een enorm salamanderachtig roofdier met scherpe tanden bestond
Fossielen tonen aan dat er vóór de dinosauriërs een enorm salamanderachtig roofdier met scherpe tanden bestond  Afbeelding:Illustratie van een Tatooine-planeet ter grootte van de aarde
Afbeelding:Illustratie van een Tatooine-planeet ter grootte van de aarde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

