
Wetenschap
Wat zou de lading van stabiele ionenzwavel zijn?
De stabiele ionenlading van zwavel is -2 .
Dit is waarom:
* Sulphur's Electron Configuration: Zwavel heeft 16 elektronen, met de configuratie:2, 8, 6. Dit betekent dat het 6 elektronen heeft in de buitenste schaal (valentie -elektronen).
* octetregel: Atomen hebben de neiging om elektronen te winnen of te verliezen om een volledige buitenste schaal van 8 elektronen (octetregel) te bereiken.
* Sulphur's voorkeur: Om een octet te bereiken, geeft zwavel de voorkeur aan * * 2 elektronen, wat het een lading van -2 geeft. Dit vormt het sulfide -ion (S²⁻).
Zwavel kan ook andere ionen vormen, zoals S⁴⁺, maar -2 is de meest stabiele en gemeenschappelijke vorm.
 Ontbossing in Brazilië zal moeilijk te stoppen zijn, maakt niet uit wie de leiding heeft
Ontbossing in Brazilië zal moeilijk te stoppen zijn, maakt niet uit wie de leiding heeft Welkom in het nieuwe Meghalayan-tijdperk - hier past het bij de rest van de geologische geschiedenis van de aarde
Welkom in het nieuwe Meghalayan-tijdperk - hier past het bij de rest van de geologische geschiedenis van de aarde Het effect van overmatig ijzer in planten
Het effect van overmatig ijzer in planten  Onderzoek naar ecologische en technologische effecten op cultuurevolutie op verschillende ruimtelijke schalen
Onderzoek naar ecologische en technologische effecten op cultuurevolutie op verschillende ruimtelijke schalen Rechter herstelt boorverbod uit Obama-tijdperk in Noordpoolgebied
Rechter herstelt boorverbod uit Obama-tijdperk in Noordpoolgebied
Hoofdlijnen
- Wat is een regeling in de microbiologie?
- Bevroren bezittingen:wie krijgt de embryo’s als een koppel uit elkaar gaat?
- Wat is de studie van dier- en plantenweefsels?
- Welke functie is in motorische eiwitten alle drie soorten spierweefsel?
- Hoe balsemen werkt
- Kan B genotype trouwen met een a en o negatief produceren?
- RNA-ontdekking kan de plantwarmte helpen verhogen, droogtetolerantie
- Wat is het verschil tussen actieve en passieve transportprocessen?
- Wat beschrijft het beste hoe chromosomen tijdens mitose naar de polen van de spil bewegen?
- Wetenschappers stellen een nieuwe technologie voor voor het maken van microstructuren van magneten

- Onderzoekers ontwikkelen een vast materiaal met mobiele deeltjes die reageren op de omgeving

- Onderzoekers ontdekken methode om kankerverwekkende formaldehydeafgifte uit hout in huis te beheersen

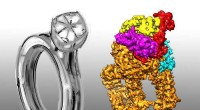
- Team rapporteert diamanten ringarchitectuur van een eiwitcomplex
- Onderzoekers gebruiken 3D-printen om kennis over microbiële gemeenschappen te vergroten

 Planten evolueren geuren en kleuren om dieren aan te trekken voor zaadverspreiding
Planten evolueren geuren en kleuren om dieren aan te trekken voor zaadverspreiding  Hoe werkt een GPS-zender bij het bestuderen van plaatbewegingen?
Hoe werkt een GPS-zender bij het bestuderen van plaatbewegingen?  Hoewel de lucht vol stikstof zit, kunnen organismen deze niet gemakkelijk gebruiken. Wat veranderde er voordat het door levende wezens werd gebruikt?
Hoewel de lucht vol stikstof zit, kunnen organismen deze niet gemakkelijk gebruiken. Wat veranderde er voordat het door levende wezens werd gebruikt?  Bestrijding van kunstmatige trilhaartjes met magnetische velden en licht
Bestrijding van kunstmatige trilhaartjes met magnetische velden en licht Hoeveel sterrenbeelden worden vandaag door astronomen erkend?
Hoeveel sterrenbeelden worden vandaag door astronomen erkend?  Wat zijn enkele geleidelijke veranderingen in het aardoppervlak?
Wat zijn enkele geleidelijke veranderingen in het aardoppervlak?  Wat is de energiebron die warmte uit rotsen haalt?
Wat is de energiebron die warmte uit rotsen haalt?  India's vuurwerkcentrum getroffen door anti-vervuilingsactie
India's vuurwerkcentrum getroffen door anti-vervuilingsactie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

