
Wetenschap
Wat is de moleculaire formule voor verbinding die 30,4 procent stikstof en 69,6 zuurstof bevat door massa met een molair van 92,0 g?
1. Bepaal de empirische formule:
* Ga uit van een 100 g monster: Dit maakt de berekeningen eenvoudiger. In een 100 g monster heb je 30,4 g stikstof (N) en 69,6 g zuurstof (O).
* Massa omzetten in mollen:
* Mol n =30,4 g / 14.01 g / mol (molmassa van n) ≈ 2,17 mol
* Mol O =69,6 g / 16,00 g / mol (molmassa van O) ≈ 4,35 mol
* Zoek de eenvoudigste verhouding tussen het hele nummer: Verdeel beide molwaarden door de kleinere (2.17 mol):
* N:2.17 / 2.17 =1
* O:4.35 / 2.17 ≈ 2
* De empirische formule is no₂.
2. Bepaal de moleculaire formule:
* Bereken de empirische formulemassa: No₂ heeft een massa van 14,01 g/mol + (2 x 16,00 g/mol) =46.01 g/mol.
* Zoek de verhouding tussen de molaire massa en de empirische formulemassa: 92.0 g/mol/46.01 g/mol ≈ 2
* Vermenigvuldig de subscripts in de empirische formule met deze verhouding: No₂ * 2 = n₂o₄
Daarom is de moleculaire formule van de verbinding n₂o₄.
 Waarom de COP26-overeenkomst moeite zal hebben om het wereldwijde bosverlies tegen 2030 terug te draaien
Waarom de COP26-overeenkomst moeite zal hebben om het wereldwijde bosverlies tegen 2030 terug te draaien Voor de beste aerosolgegevens, ARM omarmt harmonie
Voor de beste aerosolgegevens, ARM omarmt harmonie Hoe beïnvloedt sediment ecosystemen?
Hoe beïnvloedt sediment ecosystemen?  Nauwkeurigere detectie van hotspotclusters geeft nieuwe inzichten in het gedrag van luchtvervuiling
Nauwkeurigere detectie van hotspotclusters geeft nieuwe inzichten in het gedrag van luchtvervuiling Hoe groeit uw groene daktuin?
Hoe groeit uw groene daktuin?
Hoofdlijnen
- Wat heeft de vorm van een peer en heeft twee genomen? Controleer de vijver
- Hoe worden cellen genoemd die gedurende een langere periode in een specifiek bindweefseltype verblijven?
- Hommels kunnen volgens de Californische instandhoudingswet als vissen worden geclassificeerd, zegt de rechtbank
- Welk het oude organisme maakte het grootste deel van de zuurstof?
- Hoeveel dennen met bloed bevat het menselijk lichaam?
- Hoe weten planten hoe groot ze moeten worden?
- Is een boombiotische factor?
- Wat bevatten groene organellen in plantencellen die voedsel maken?
- Uw smartphone is mogelijk gelinkt aan krokodillenaanvallen in Indonesië
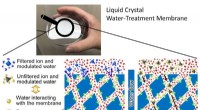
- Zeer selectieve membranen:onderzoekers ontdekken hoe water zijn eigen filtratie kan beïnvloeden
- Een zelfgenezend, waterafstotende coating die ultra duurzaam is

- Glas verwerken als een polymeer

- Onderzoekers vereenvoudigen en stroomlijnen de organische chemische synthese drastisch

- Nieuwe lijm plakt gemakkelijk, houdt sterk, en is een gas om uit elkaar te trekken

 Wat is de empirische formule voor kaliumnitride van ionische verbinding?
Wat is de empirische formule voor kaliumnitride van ionische verbinding?  FedEx klaagt Amerikaanse overheid aan wegens exportregels in Huawei-zaak
FedEx klaagt Amerikaanse overheid aan wegens exportregels in Huawei-zaak Hoe wordt de studie van materie en energie genoemd?
Hoe wordt de studie van materie en energie genoemd?  Wie heeft de sterrenkaart uitgevonden?
Wie heeft de sterrenkaart uitgevonden?  Hoe u vlakglas perfect om hoeken buigt
Hoe u vlakglas perfect om hoeken buigt Onderzoekers laten zien dat opgewonden elektronen het scheve rooster van perovskiet-nanokristallen rechttrekken
Onderzoekers laten zien dat opgewonden elektronen het scheve rooster van perovskiet-nanokristallen rechttrekken  Consumenten gaven minder uit aan snoep en desserts bij het online winkelen
Consumenten gaven minder uit aan snoep en desserts bij het online winkelen Wat voor soort energie wordt opgeslagen als u het stoelkussen comprimeert?
Wat voor soort energie wordt opgeslagen als u het stoelkussen comprimeert?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

