
Wetenschap
Als atomen van chloor en fluor gemakkelijk een extra elektron aannemen, voorspellen welke andere soorten ook deze chemische eigenschap hebben?
Dit is de reden waarom halogenen deze neiging hebben:
* Elektronenconfiguratie: Halogenen hebben 7 elektronen in hun buitenste schaal. Ze zijn slechts één elektron tekort bij het bereiken van een stabiele, volledige buitenste schaal (8 elektronen).
* elektronegativiteit: Halogenen zijn zeer elektronegatief, wat betekent dat ze een sterke aantrekkingskracht hebben op elektronen.
Daarom zullen andere elementen in groep 17 (halogenen) ook gemakkelijk een extra elektron aannemen. Deze omvatten:
* bromine (br)
* jodium (i)
* astatine (AT)
Opmerking: Hoewel Astatine een halogeen is, is het radioactief en heeft het zeer beperkte toepassingen.
Laat het me weten als je nog andere vragen hebt over chemie!
 Welke kleur moet de vlam op een gasketel zijn?
Welke kleur moet de vlam op een gasketel zijn?  Wanneer u water toevoegt aan een glas ijsthee en kleur wordt verlicht, is het fysische of chemische verandering?
Wanneer u water toevoegt aan een glas ijsthee en kleur wordt verlicht, is het fysische of chemische verandering?  Welke sourrounds een elektrische lading?
Welke sourrounds een elektrische lading?  Wat is het uiterlijk van de verbinding?
Wat is het uiterlijk van de verbinding?  Wat is de eigenschap waarmee vers gesneden oppervlak van een metaal schijnt?
Wat is de eigenschap waarmee vers gesneden oppervlak van een metaal schijnt?
 Klimaatverandering zal de komende decennia miljoenen verdringen - landen moeten zich nu voorbereiden om hen te helpen
Klimaatverandering zal de komende decennia miljoenen verdringen - landen moeten zich nu voorbereiden om hen te helpen Onderschatten we microplastics in het mariene milieu?
Onderschatten we microplastics in het mariene milieu? Timber Wolf-aanpassingen
Timber Wolf-aanpassingen  Seychellen-chef roept vanuit de diepte voor bescherming van de oceaan
Seychellen-chef roept vanuit de diepte voor bescherming van de oceaan Nieuwe kaarten van Groenland tonen meer gletsjers die gevaar lopen
Nieuwe kaarten van Groenland tonen meer gletsjers die gevaar lopen
Hoofdlijnen
- Wat is een symbiotische relatie waarin het ene organisme ten goede komt aan het andere dat niet wordt beïnvloed?
- Wat betekent monster in de wetenschap?
- Wat eten genets?
- Wat zijn de componenten die betrokken zijn bij transcriptie?
- De spaarzame genentheorie suggereert dat?
- Lead veiligheidsrichtlijnen ontbreken voor stadsboeren in veel grote Amerikaanse steden
- Hoe werkt deconcentratie in de biologie?
- Een buis gevormd door de innerlijke uitbreiding van het celmembraan wordt A genoemd?
- Wat zijn de 2 belangrijkste verschillen tussen dieren- en plantencellen?
- Eenvoudige entropieën voor gecompliceerde moleculen

- Waterdichte capsules voor doelgerichte toediening van medicijnen

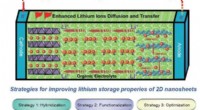
- Regulering van tweedimensionale nanomaterialen voor lithium-ionbatterijen
- Make like a leaf:onderzoekers ontwikkelen methode om koolstofdioxide om te zetten

- Onthulling wat de kristalgroei regelt

 Wetenschappers zeggen dat Harvey het doorweekte teken kan zijn van toekomstige stormen
Wetenschappers zeggen dat Harvey het doorweekte teken kan zijn van toekomstige stormen Dodelijke superstormen in India doden bijna 150
Dodelijke superstormen in India doden bijna 150 Decodering van tornado's infrageluidsgolven
Decodering van tornado's infrageluidsgolven Natuurkundigen induceren supergeleiding in niet-supergeleidende materialen
Natuurkundigen induceren supergeleiding in niet-supergeleidende materialen Waar komen uw online winkelretouren terecht? In de prullenbak, zo blijkt uit nieuw onderzoek
Waar komen uw online winkelretouren terecht? In de prullenbak, zo blijkt uit nieuw onderzoek  Demonstratie van snelle SOT-MRAM-geheugencel die compatibel is met 300 mm Si CMOS-technologie
Demonstratie van snelle SOT-MRAM-geheugencel die compatibel is met 300 mm Si CMOS-technologie Verkiezingen buiten de cyclus resulteren in minder representatieve lokale overheden
Verkiezingen buiten de cyclus resulteren in minder representatieve lokale overheden Wat zijn platte botten in het menselijk lichaam?
Wat zijn platte botten in het menselijk lichaam?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

