
Wetenschap
Wanneer een atoom van chloor vormt ionische binding met chloor?
Chlooratomen niet Vorm ionische bindingen met elkaar. Dit is waarom:
* elektronegativiteit: Chloor heeft een relatief hoge elektronegativiteit, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen.
* Vergelijkbare elektronegativiteit: Wanneer twee chlooratomen binden, zijn hun elektronegativiteiten hetzelfde. Dit betekent dat ze een gelijke trek hebben op gedeelde elektronen.
* Covalente binding: In plaats van dat een elektron wordt overgedragen (ionische binding), worden de elektronen gelijk gedeeld, wat resulteert in een covalente binding . Dit creëert een diatomee chloormolecuul (CL₂).
Samenvattend: Chlooratomen binden covalent om Cl₂ -moleculen te vormen, niet ionisch.
 Vinden zuren of basen sneller?
Vinden zuren of basen sneller?  Onderzoekers ontwikkelen nieuwe manier om verontreinigende stoffen uit water te verwijderen
Onderzoekers ontwikkelen nieuwe manier om verontreinigende stoffen uit water te verwijderen Noem het proces waar een vaste stof in vloeistof afbreekt?
Noem het proces waar een vaste stof in vloeistof afbreekt?  Waarom heeft magnesium een lager smelt- en kookpunt dan calciumstrontium andere leden die onder magnesium aanwezig zijn?
Waarom heeft magnesium een lager smelt- en kookpunt dan calciumstrontium andere leden die onder magnesium aanwezig zijn?  Wat is de moleculaire vorm van een watermolecuul en waarom?
Wat is de moleculaire vorm van een watermolecuul en waarom?
 Waarschijnlijkheid dat schepen van verschillende polaire scheepscategorieën vast komen te zitten in ijs in Arctische wateren
Waarschijnlijkheid dat schepen van verschillende polaire scheepscategorieën vast komen te zitten in ijs in Arctische wateren Tyfoon Hato laat 16 doden achter na geseling Zuid-China
Tyfoon Hato laat 16 doden achter na geseling Zuid-China 5 Aardse feiten om de geest van uw kind te verbazen
5 Aardse feiten om de geest van uw kind te verbazen  Het wel en wee van een megameer
Het wel en wee van een megameer Bodem is de sleutel tot de geschiedenis (en toekomst) van de aarde
Bodem is de sleutel tot de geschiedenis (en toekomst) van de aarde
Hoofdlijnen
- Wat zijn de belangrijkste groepen domein archaea?
- Wat betekent co-dominantie in genetica?
- Nieuw onderzoek toont aan dat micro-evolutie kan worden gebruikt om te voorspellen hoe evolutie op veel langere tijdschalen werkt
- Hoe handhaaft het plasmamembraan homeostase?
- Wat zijn een of twee nucleotiden die in een bepaalde mutatie worden veranderd?
- Welk membraangebonden organel wordt gebruikt om nucleïnezuren in een eukaryotische cel op te slaan?
- In het verleden werpen helpt de toekomst van de visserij te onthullen
- Evolutie hoe werkt
- Wat doet een celmembraan in plantencel?
- Innovatieve biogebaseerde luchtfilter kan luchtfiltratie transformeren, mogelijk allergenen in de lucht binnenshuis verminderen

- Recente vorderingen in NMR-onderzoeken in vaste toestand van zeolietkatalysatoren

- Spinzijde kan worden gebruikt als robotspier

- Wetenschap onthult geheimen van een mummieportret

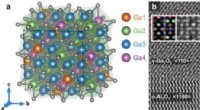
- Galliumoxidekristalcomplexiteit getemd door machine learning
 Wat zijn gewelddadige explosies van zonnevlekken waarin gas en enorme hoeveelheden energie in de ruimte in de zon schiet.
Wat zijn gewelddadige explosies van zonnevlekken waarin gas en enorme hoeveelheden energie in de ruimte in de zon schiet.  Hoeveel is een energie in joules?
Hoeveel is een energie in joules?  Is lichte energie schadelijk voor de mens?
Is lichte energie schadelijk voor de mens?  Hoe berekent u de omvang van de normale kracht?
Hoe berekent u de omvang van de normale kracht?  Identificeer de beste tijd van de dag om elke hernieuwbare energiebronnen te verkrijgen?
Identificeer de beste tijd van de dag om elke hernieuwbare energiebronnen te verkrijgen?  Hoe classificeren geologen een massabeweging?
Hoe classificeren geologen een massabeweging?  Hoe hoog is een object van 3,00 kg met 300J energie?
Hoe hoog is een object van 3,00 kg met 300J energie?  Waterstofkracht komt een stap dichterbij
Waterstofkracht komt een stap dichterbij
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

