
Wetenschap
Waarom heeft het fluoratoom een valentie -elektron gekregen?
Dit is de reden waarom fluor een elektron wil krijgen:
* stabiliteit: Atomen zijn het meest stabiel wanneer hun buitenste elektronenschil (valentieschaal) vol is.
* Fluor's Electron Configuration: Fluor heeft 9 elektronen:2 in de eerste schaal en 7 in de tweede. Om een volledige buitenste schaal te hebben, heeft deze 8 elektronen nodig.
* een elektron winnen: Door één elektron te winnen, bereikt fluor een volledige buitenste schaal en wordt hij een fluoride-ion (F-). Deze configuratie is stabieler en energetisch gunstig.
Zie het zo:fluor is als een puzzelstuk met één ontbrekende hoek. Door een elektron te winnen, voltooit het de puzzel en wordt het een stabiel, compleet stuk.
 Wat maakt waterstofperoxide en tangdrinkpoeder?
Wat maakt waterstofperoxide en tangdrinkpoeder?  Waarom worden estersverbindingen ook derivaten van carbonzuur genoemd?
Waarom worden estersverbindingen ook derivaten van carbonzuur genoemd?  Hoe wordt het proces genoemd wanneer een vloeistof van hoge concentratie naar lage concentratie gaat?
Hoe wordt het proces genoemd wanneer een vloeistof van hoge concentratie naar lage concentratie gaat?  Waar bevinden zich alkalimetalen in het periodiek systeem en hun groepsnummer?
Waar bevinden zich alkalimetalen in het periodiek systeem en hun groepsnummer?  Is Freon een vaste vloeistof of gas?
Is Freon een vaste vloeistof of gas?
 Zijn de vogels die uit de lucht vielen in Arkansas op nieuwe 2011 gekoppeld aan Falling Louisiana en Argentinië?
Zijn de vogels die uit de lucht vielen in Arkansas op nieuwe 2011 gekoppeld aan Falling Louisiana en Argentinië?  Steden in Californië doen het meest aan klimaatactie
Steden in Californië doen het meest aan klimaatactie Zwaartekrachtmissie onthult nog steeds verborgen geheimen
Zwaartekrachtmissie onthult nog steeds verborgen geheimen Simulaties tonen aan dat magnetisch veld 10 keer sneller kan veranderen dan eerder werd gedacht
Simulaties tonen aan dat magnetisch veld 10 keer sneller kan veranderen dan eerder werd gedacht Waarom slagen we er nog steeds niet in om de ontbossing te stoppen?
Waarom slagen we er nog steeds niet in om de ontbossing te stoppen?
Hoofdlijnen
- Welk orgaan is nodig om door mensen te worden uitgevoerd voor uitscheiding?
- Met welke organel zijn eiwitten gesynthetiseerd?
- Hoe een moleculaire schakelaar de groei van plantenorganen vormgeeft
- Wat zijn nieuwe gencombinaties?
- Het voorbehandelen van de grond met ethanol beschermt planten tegen droogte
- De vier eigenschappen van spiercellen
- Hoe definieer je haat?
- Hoe bewijst Louis Pasteur zijn kiemtheorie van ziekten?
- Waarom zou een kind te veel enzymen in bloed hebben?
- Nieuw kristallijn oxide kan het probleem van oververhitting in composietmaterialen oplossen

- Nieuwe behandeling ontsluit potentieel voor het bakken van frambozen

- Nieuwe verbinding kan fotodynamische therapie voor kanker verbeteren

- Door ontwerp:van afval naar de volgende generatie koolstofvezel

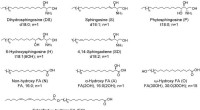
- Onderzoekers beschrijven het volledige scala aan ceramiden dat wordt aangetroffen in de bovenste laag van de menselijke huid
 Welke minerale afzettingen zijn er in de Filippijnen?
Welke minerale afzettingen zijn er in de Filippijnen?  Overstromingen in Zuid-Brazilië hebben 600.000 mensen op de vlucht gedreven – dit is de reden waarom deze regio in de toekomst waarschijnlijk steeds extremere regen zal zien
Overstromingen in Zuid-Brazilië hebben 600.000 mensen op de vlucht gedreven – dit is de reden waarom deze regio in de toekomst waarschijnlijk steeds extremere regen zal zien  Wat is een goede samenvatting voor de vulkaan van het wetenschapsproject?
Wat is een goede samenvatting voor de vulkaan van het wetenschapsproject?  Wat is de warmte van de vorming siliciumgas?
Wat is de warmte van de vorming siliciumgas?  Sneller betere magneten vinden met 3D-prototyping van metaalprinten
Sneller betere magneten vinden met 3D-prototyping van metaalprinten De beste landbouwpraktijken voor bodemgezondheid verschillen per regio
De beste landbouwpraktijken voor bodemgezondheid verschillen per regio Russisch, Amerikaanse functionarissen zeggen dat samenwerking in de ruimte sterk blijft
Russisch, Amerikaanse functionarissen zeggen dat samenwerking in de ruimte sterk blijft Hoe ver is de maan van Mars?
Hoe ver is de maan van Mars?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

