
Wetenschap
Wanneer natrium en chloor een ionische binding vormen die ze maken?
Hier is hoe het werkt:
* natrium (na) is een metaal en heeft één valentie -elektron (een elektron in de buitenste schaal). Het wil dit elektron verliezen om een stabiele elektronenconfiguratie te bereiken.
* chloor (Cl) is een niet -metaal en heeft zeven valentie -elektronen. Het wil één elektron krijgen om een stabiele elektronenconfiguratie te bereiken.
Wanneer natrium en chloor reageren, verliest natrium zijn valentie -elektron aan chloor. Dit resulteert in:
* Natriumion (Na+) - Natrium verliest een elektron en wordt positief geladen.
* chloride-ion (Cl-) - Chloor krijgt een elektron en wordt negatief geladen.
De tegenovergestelde ladingen van de natrium- en chloride -ionen trekken elkaar aan en vormen een ionische binding . Deze binding houdt de ionen bij elkaar in een kristalroosterstructuur en vormt natriumchloride (NaCl).
 Moet het EU-verbod op de import van zeehondenproducten standhouden?
Moet het EU-verbod op de import van zeehondenproducten standhouden?  Humanitaire forensische wetenschappers sporen de vermiste, identificeer de doden en troost de levenden
Humanitaire forensische wetenschappers sporen de vermiste, identificeer de doden en troost de levenden Wat is het proces door welke polaire stoffen in water oplossen, worden uit elkaar getrokken?
Wat is het proces door welke polaire stoffen in water oplossen, worden uit elkaar getrokken?  Wat is een waterstofkernen?
Wat is een waterstofkernen?  Hoe beïnvloedt een remmer de snelheid van chemische reactie?
Hoe beïnvloedt een remmer de snelheid van chemische reactie?
Hoofdlijnen
- Kan bionisch lezen je sneller laten lezen?
- Welke organel tagt eiwitten?
- Hoe is de bevruchting anders dan de ontwikkeling van het embryo?
- De griezelige vraag van de vogelgriep:hoe miljoenen pluimvee te doden
- Welk aminozuur is aanwezig in wateroplosbaar globulair eiwit?
- Wat zijn 10 takken van wetenschap en definiëren ze elk?
- Wat is een verzameling organen die een specifieke functie voor het lichaam uitvoeren?
- Welk organisme kan de vorm veranderen?
- Een probioticum voor onze longen? Nieuw onderzoek roept vragen op over de toekomst van de behandeling van COVID-19
- Duurzame polymeren maken van geurige moleculen

- Onderzoek toont aan hoe kleine compartimenten aan cellen vooraf konden gaan

- Een theoretische studie verklaart de natuurlijke selectie van eiwitten
- Hoe een functionele moleculaire machine te coderen?
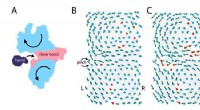
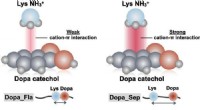
- Het geheim van de plakkerigheid van mosselen onder water
 Wat gebeurt er met een metamorfe rots als het is verweerd?
Wat gebeurt er met een metamorfe rots als het is verweerd?  Is Wall Street enthousiast over Yahoo's Microsoft-pact?
Is Wall Street enthousiast over Yahoo's Microsoft-pact?  Wat is het focuspunt van een vulkaan?
Wat is het focuspunt van een vulkaan?  Is Mars de 1 2 3 van de zon?
Is Mars de 1 2 3 van de zon?  Lunaire goudkoorts kan conflicten op de grond veroorzaken als we nu niet handelen - nieuw onderzoek
Lunaire goudkoorts kan conflicten op de grond veroorzaken als we nu niet handelen - nieuw onderzoek Wat is de vorm en energie geassocieerd met de positie van beweging een object?
Wat is de vorm en energie geassocieerd met de positie van beweging een object?  Nieuw complex dat reageert met nitril - een sleutel om down-regulatie van kanker-enzymen mogelijk te maken
Nieuw complex dat reageert met nitril - een sleutel om down-regulatie van kanker-enzymen mogelijk te maken Wat betreft de productie en de daaropvolgende fusie van gameten?
Wat betreft de productie en de daaropvolgende fusie van gameten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

