
Wetenschap
Hoe wordt de binding tussen waterstofatomen weergegeven in elk model van een molecuul?
1. Lewis Dot Structures
* Representatie: Een enkele lijn (-) die de twee waterstofatomen verbindt.
* Verklaring: Dit model richt zich op het delen van elektronen tussen de atomen. De lijn vertegenwoordigt een enkele covalente binding, waarbij elk waterstofatoom één elektron bijdraagt aan het gedeelde paar.
2. Ball-and-stick modellen
* Representatie: Twee bollen (die waterstofatomen vertegenwoordigen) verbonden door een stok.
* Verklaring: Dit model benadrukt de ruimtelijke opstelling van atomen. De bollen vertegenwoordigen de atoomkernen en de stok vertegenwoordigt de binding tussen hen.
3. Space-vulmodellen
* Representatie: Twee bollen (die waterstofatomen vertegenwoordigen) aanraken en overlappen.
* Verklaring: Dit model benadrukt de elektronenwolken rond de atomen. De bollen zijn geschaald om de elektronendichtheid weer te geven, waardoor een meer realistische weergave van de grootte van het atoom en de manier waarop ze omgaan.
4. Moleculaire orbitale diagrammen
* Representatie: Overlappende atomaire orbitalen (1s orbitalen in het geval van waterstof) die een moleculaire orbitaal vormen.
* Verklaring: Dit model is een meer geavanceerde weergave die de werkelijke verbindingsinteractie tussen atomen weergeeft. De overlappende orbitalen vertegenwoordigen de gedeelde elektronen die de covalente binding creëren.
Sleutelpunt: De weergave van een waterstofbinding in elk model hangt af van het detailniveau en de informatie die het beoogt over te brengen.
Laat het me weten als je een specifiek voorbeeld wilt voor een bepaald molecuul (zoals H2O of H2).
Hoofdlijnen
- De structurele verschillen tussen zenuwen en bloedvaten
- Het eerste genetische materiaal was waarschijnlijk?
- Welk werk doet een cellichaam?
- Wat is een eigenschap die wordt bestuurd door drie of meer allelen?
- Welk deel van het centrale zenuwstelsel dat de meeste functies in het lichaam regelt?
- De overdracht van genen tijdens bacteriële conjugatie omvat rigide buisvormige aanhangsels met de naam Wat?
- Is het waar dat sommige bacteriën geen ziekteverwekkers zijn?
- Hoe trotseren levende cellen de natuurlijke trends van het universum?
- Wat zijn wetenschappelijke inhoudsverklaringen?
- Onderzoekers kijken naar schimmel om licht te werpen op kanker

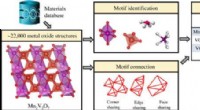
- Structuurmotiefgericht leerkader voor anorganische kristallijne systemen
- Leviathan-polymeerborstel gemaakt met E. coli houdt bacteriën op afstand

- Creature-functie:draaiende scheuren geven dieren taaiheid van superhelden

- Stabiliserende 2-D gelaagde perovskieten voor fotovoltaïsche zonne-energie:een verdedigingsmuur opzetten

 AI-onderzoek biedt meer ogen en oren voor zoek- en reddingsmissies
AI-onderzoek biedt meer ogen en oren voor zoek- en reddingsmissies Cadmium:het zeer giftige metaal dat de wereld aandrijft
Cadmium:het zeer giftige metaal dat de wereld aandrijft  Wat is het abstracte zelfstandig naamwoord voor bijvoeglijk naamwoord warm?
Wat is het abstracte zelfstandig naamwoord voor bijvoeglijk naamwoord warm?  Bescherming voor volle zee is cruciaal om kwetsbare kustgemeenschappen te beschermen - nieuw onderzoek
Bescherming voor volle zee is cruciaal om kwetsbare kustgemeenschappen te beschermen - nieuw onderzoek Hoe je het niets uit balans kunt brengen
Hoe je het niets uit balans kunt brengen  De app voor het traceren van contacten waarschuwt voor blootstelling aan COVID-19 en beschermt tegelijkertijd de privacy
De app voor het traceren van contacten waarschuwt voor blootstelling aan COVID-19 en beschermt tegelijkertijd de privacy Wat is de verhoging van de Arabische Zee?
Wat is de verhoging van de Arabische Zee?  Ik ben de enorme bergketens onder water die aanwezig zijn in elke oceaan en cirkel aarde?
Ik ben de enorme bergketens onder water die aanwezig zijn in elke oceaan en cirkel aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


