
Wetenschap
Hoe zou u deze chemische vergelijking waterige oplossingen van bariumchloride en natriumfluoride schrijven, worden gemengd om een neerslag waterig chloride te vormen?
1. Evenwichtige chemische vergelijking:
BACL₂ (aq) + 2NAf (aq) → baf₂ (s) + 2nacl (aq)
Verklaring:
* (aq) geeft aan dat de stof is opgelost in water (waterige oplossing).
* (s) geeft aan dat de stof een vaste stof is (neerslag).
* coëfficiënten: De getallen voor elke verbinding (1, 2, 1, 2) balanceren de vergelijking en zorgen voor hetzelfde aantal atomen van elk element aan beide zijden van de reactie.
2. Ionische vergelijking:
Ba²⁺ (aq) + 2cl⁻ (aq) + 2na⁺ (aq) + 2f⁻ (aq) → baf₂ (s) + 2na⁺ (aq) + 2cl⁻ (aq)
* In de ionische vergelijking scheiden we de oplosbare ionische verbindingen in hun individuele ionen.
3. Netto ionische vergelijking:
Ba²⁺ (aq) + 2f⁻ (aq) → baf₂ (s)
* De netto ionische vergelijking toont alleen de ionen die direct deelnemen aan de vorming van het neerslag. De toeschouwersionen (Na⁺ en CL⁻) die aan beide zijden van de reactie aanwezig zijn, worden verwijderd.
Sleutelpunt: De vorming van bariumfluoride (BAF₂), een onoplosbare vaste stof, is de drijvende kracht achter deze reactie. Dit is de reden waarom de reactie verloopt en een neerslag wordt gevormd.
 Hoe combineren atomen om verbindingen te maken?
Hoe combineren atomen om verbindingen te maken?  De C-H-bindingen in koolwaterstoffen verbreken om complexe organische moleculen te synthetiseren
De C-H-bindingen in koolwaterstoffen verbreken om complexe organische moleculen te synthetiseren Hoe de ozonlaag
Hoe de ozonlaag  Fossiele brandstoffen kunnen nog steeds bijdragen aan luchtvervuiling, zelfs als de auto is uitgeschakeld
Fossiele brandstoffen kunnen nog steeds bijdragen aan luchtvervuiling, zelfs als de auto is uitgeschakeld Wat is een wetenschappelijke verbinding?
Wat is een wetenschappelijke verbinding?
 Soorten paddenstoelen in South Carolina
Soorten paddenstoelen in South Carolina  SwRI-ontwikkelde satellieten gaan tweede fase van operaties in
SwRI-ontwikkelde satellieten gaan tweede fase van operaties in NASA vindt Tropical Storm Dolphin aan het zwemmen
NASA vindt Tropical Storm Dolphin aan het zwemmen Magnetronbehandeling is een goedkope manier om zware metalen uit gezuiverd afvalwater te verwijderen
Magnetronbehandeling is een goedkope manier om zware metalen uit gezuiverd afvalwater te verwijderen Onderzoekers zien noodzaak tot actie tegen bosbrandrisico
Onderzoekers zien noodzaak tot actie tegen bosbrandrisico
Hoofdlijnen
- Wat bepaalt welke eiwitten de cel maakt?
- Wat is de structuur van een erytrocyt?
- Hoe vinden wetenschappers informatie over de structuur?
- De wetenschap zegt:waarom wetenschappers planten- en dierengenomen waarderen
- Heeft een virus DNA?
- Leef snel, sterf jong:signaaldetectietheorie bijwerken
- Experiment-ID's invloed van antibiotica, isolatie op gastheerbacteriën
- Hoe een moleculair signaal plantencellen helpt beslissen wanneer ze olie moeten maken
- Wat is de basiseenheid van reproductie?
- Een betere manier om watermoleculen te splitsen om waterstof te produceren met behulp van zonlicht

- Een microscoop voor iedereen:onderzoekers ontwikkelen open-source optische toolbox
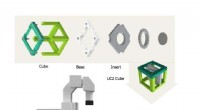
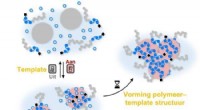
- Het polymerisatieproces in- en uitschakelen met een schakelbare sjabloon
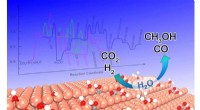
- Water zou de activiteit en selectiviteit van koolstofdioxidereductie kunnen moduleren
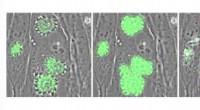
- Onderzoek naar parasieten warmt op
 De meest voorkomende mineralen in clastic sedimentaire rotsen zijn waarschijnlijk?
De meest voorkomende mineralen in clastic sedimentaire rotsen zijn waarschijnlijk?  Wat is het oudste object in ons zonnestelsel?
Wat is het oudste object in ons zonnestelsel?  Hoe verschillen cellen die zich aan het einde van de meiose vormen van de cellen die tijdens de mitose worden gevormd?
Hoe verschillen cellen die zich aan het einde van de meiose vormen van de cellen die tijdens de mitose worden gevormd?  Welke elementen vormen 90 procent van het menselijk lichaam?
Welke elementen vormen 90 procent van het menselijk lichaam?  Hoe fruit zijn opvallende kleuren kreeg
Hoe fruit zijn opvallende kleuren kreeg  Hoe fok je fossiele draak in Dragoncity?
Hoe fok je fossiele draak in Dragoncity?  Waarom reizen sommige golven in een vaccuüm, terwijl anderen alleen via medium kunnen?
Waarom reizen sommige golven in een vaccuüm, terwijl anderen alleen via medium kunnen?  NASA analyseert kortstondige cycloon in de Golf van Bengalen
NASA analyseert kortstondige cycloon in de Golf van Bengalen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

