
Wetenschap
Wat is de moleculaire geometrie van dihydrogen monosulfide?
Dihydrogen monosulfide (H₂s) heeft een gebogen of Angular moleculaire geometrie.
Dit is waarom:
* centraal atoom: Zwavel (s) is het centrale atoom.
* valentie -elektronen: Zwavel heeft 6 valentie -elektronen en elke waterstof heeft 1.
* binding: Zwavel vormt twee enkele bindingen met de twee waterstofatomen.
* eenzame paren: Zwavel heeft twee eenzame paren elektronen.
* vSEPR -theorie: De twee eenzame paren op zwavel stoten de bindingsparen af en duwen de waterstofatomen dichter bij elkaar.
Deze opstelling van twee bindingsparen en twee eenzame paren rond het centrale atoom resulteert in een gebogen of hoekige vorm met een bindingshoek iets minder dan 109,5 graden.
 Hoe worden regenbogen gevormd? De wetenschap achter de kleuren
Hoe worden regenbogen gevormd? De wetenschap achter de kleuren  Beschrijf welke rol die de omgeving in theorie speelt?
Beschrijf welke rol die de omgeving in theorie speelt?  Als je landt, kun je dan staan? Eenjarige missie-videominiserie:functionele prestaties
Als je landt, kun je dan staan? Eenjarige missie-videominiserie:functionele prestaties  We keken naar 1, 154 klimaatwetenschappelijke resultaten en geen bewijs gevonden van publicatiebias
We keken naar 1, 154 klimaatwetenschappelijke resultaten en geen bewijs gevonden van publicatiebias Nieuwe COVID-relevante richtlijnen voor brandveiligheid en noodevacuatie voor intensive care-afdelingen voor 2021 gelanceerd
Nieuwe COVID-relevante richtlijnen voor brandveiligheid en noodevacuatie voor intensive care-afdelingen voor 2021 gelanceerd
Hoofdlijnen
- Waar zijn de dikke eiwitfilamenten in cel van gemaakt?
- Wat is een substraat dat in een enzymgebied past?
- Wat is een natuurlijke organisatie?
- Waar komt jouw inktvis vandaan? Hoogstwaarschijnlijk ongereguleerde wateren, volgens een nieuwe internationale studie
- Uit onderzoek blijkt hoe twee stammen van één bacterie samen een vleesetende infectie veroorzaken
- Wie stelde het idee van overleven die fittest is een theorie -evolutie voor?
- Hoe zijn genen, DNA en chromosomen met elkaar verbonden?
- Wat is het verschil tussen pathogene microbiologie en algemene microbiologie?
- Biomechanica-team ontdekt hoe insecten hun 'botten' repareren
- 3D-printen van plastic onderdelen verbeteren
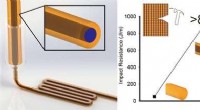
- Alles-afstotende coating kan telefoons kinderveilig maken, huizen

- Freeze frame:onderzoekers lossen op hoe cellen eiwitten ontvouwen
- Nieuwe benadering voorspelt het altijd evoluerende gedrag van glas bij verschillende temperaturen

- Nieuw materiaal kan ademhalingsdruppels uit de lucht verwijderen

 Een missie naar Mars kan zijn eigen zuurstof maken via plasmatechnologie
Een missie naar Mars kan zijn eigen zuurstof maken via plasmatechnologie Hoeveel natriumatomen vormen het element?
Hoeveel natriumatomen vormen het element?  Het proces van scheiding F mengsel kamfer en natriumchloride?
Het proces van scheiding F mengsel kamfer en natriumchloride?  Een kwantummetrologisch protocol voor het lokaliseren van niet-coöperatieve doelen in de 3D-ruimte
Een kwantummetrologisch protocol voor het lokaliseren van niet-coöperatieve doelen in de 3D-ruimte Een nieuwe kijk op schoolschorsingen:het schoolklimaat biedt een aanwijzing
Een nieuwe kijk op schoolschorsingen:het schoolklimaat biedt een aanwijzing Wat zijn de 4 genoemde krachten in de natuurkunde?
Wat zijn de 4 genoemde krachten in de natuurkunde?  Welke Griekse astronoom gebruikte observaties van de positie 's middags op zomerzonnewende Alexandrië en Syene om de omtrek aarde te bepalen?
Welke Griekse astronoom gebruikte observaties van de positie 's middags op zomerzonnewende Alexandrië en Syene om de omtrek aarde te bepalen?  Waarom blijft een vallend object dat wordt onderworpen aan de zwaartekracht niet voor altijd versnellen?
Waarom blijft een vallend object dat wordt onderworpen aan de zwaartekracht niet voor altijd versnellen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

