
Wetenschap
Wanneer HCLO oplossen in H2O?
* HCLO is een zwak zuur: Dit betekent dat het niet volledig dissocieert (uit elkaar breekt) in zijn ionen in water.
* evenwicht: De oplossing van HCLO in water vormt een evenwicht tussen de niet -gedisocieerde HCLO -moleculen en zijn ionen, hypochlorietionen (clo⁻) en hydroniumionen (H₃o⁺):
`` `
Hclo (aq) + h₂o (l) ⇌ h₃o⁺ (aq) + clo⁻ (aq)
`` `
* factoren die de ionisatie beïnvloeden: De mate van ionisatie hangt af van factoren zoals de concentratie van HCLO en de temperatuur.
Sleutelpunten:
* Niet alle HCLO -moleculen dissociëren: Een aanzienlijk deel van HCLO blijft in zijn moleculaire vorm in oplossing.
* Hypochloor zuur is een zwak zuur: Het ioniseert niet volledig als sterke zuren (bijv. HCl, Hno₃).
* evenwicht is vastgesteld: De voorwaartse en omgekeerde reacties gebeuren tegelijkertijd, wat leidt tot een evenwicht tussen de reactanten en producten.
Belangrijke opmerking: Hypochlorzuur is een krachtig desinfectiemiddel en oxidatiemiddel. Het wordt gebruikt in veel toepassingen, waaronder waterbehandeling, wondverzorging en huishoudelijke schoonmaakproducten.
 Wat zijn enkele voorbeelden van vaste vloeibare oplossingen?
Wat zijn enkele voorbeelden van vaste vloeibare oplossingen?  Koolstofdioxide en water zijn afvalproducten van welk proces?
Koolstofdioxide en water zijn afvalproducten van welk proces?  Wat is de thermische ontleding van natriumcarbonaat?
Wat is de thermische ontleding van natriumcarbonaat?  Nucleaire fusie anders dan wanneer atomen zich aansluiten om een molecuul te vormen?
Nucleaire fusie anders dan wanneer atomen zich aansluiten om een molecuul te vormen?  Hoge efficiëntie, goedkope katalysator voor waterelektrolyse
Hoge efficiëntie, goedkope katalysator voor waterelektrolyse
Hoofdlijnen
- Waarom zijn walvissen belangrijk voor uw ecosysteem?
- Wanneer bevat een menselijke cel normaal 92 chromosomen?
- Wat zijn de soorten dichte bindweefsels?
- Hoe reageren planten?
- Wat levert het nieuwe materiaal op waarop de evolutie kan inwerken b. Genetische instandhouding c. Mutaties d. Fenotypes a. Handelaar.?
- Hoe een spanningssensor een integrale rol speelt bij de uitgelijnde chromosoompartitie
- Welk bloedceltype wordt een polymorf genoemd?
- Wat maakt een leider? Aanwijzingen uit het dierenrijk
- Waarom dassen ten onrechte worden gedemoniseerd en wat we kunnen doen om te helpen
- Onderzoekers ontwikkelen dynamische sjablonen die essentieel zijn voor afdrukbare elektronicatechnologie

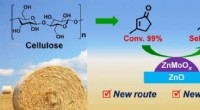
- Onderzoekers synthetiseren biobased methylcyclopentadieen met 3-methylcyclopent-2-enon
- Scholen moleculaire vissen kunnen beeldschermen verbeteren

- Wetenschappers ontwikkelen elektrochemisch platform voor celvrije synthetische biologie

- Gezien de impact van de chemiecocktail voor binnenshuis

 Hoe werkt de thermometers van de LCD -strip?
Hoe werkt de thermometers van de LCD -strip?  Verminder de angst om Engels te leren met mobiel gamen
Verminder de angst om Engels te leren met mobiel gamen Waar komen de evenaar en het tropic van kanker samen?
Waar komen de evenaar en het tropic van kanker samen?  In Ethiopië, rijkdom van moeders beter beschermd tegen kindhuwelijken dan vaders
In Ethiopië, rijkdom van moeders beter beschermd tegen kindhuwelijken dan vaders Waarom zou driefasen worden gebruikt in plaats van een enkele fase?
Waarom zou driefasen worden gebruikt in plaats van een enkele fase?  Als je tijdens een nieuwe maan aan de manen in de buurt was, zou hoeveel van aardes in zonlicht zonlicht zijn?
Als je tijdens een nieuwe maan aan de manen in de buurt was, zou hoeveel van aardes in zonlicht zonlicht zijn?  Dood door ontwerp? Ruimtelijke modellen laten zien dat natuurlijke selectie een genetisch beperkte levensduur als lineair voordeel bevoordeelt
Dood door ontwerp? Ruimtelijke modellen laten zien dat natuurlijke selectie een genetisch beperkte levensduur als lineair voordeel bevoordeelt  Hoe kan iemand een machine besturen met haar gedachten?
Hoe kan iemand een machine besturen met haar gedachten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

