
Wetenschap
Wat is het aantal covalente bindingen in 8 g methaan?
1. Bepaal de moleculaire formule van methaan:
* De chemische formule van methaan is Ch₄. Dit betekent dat elk methaanmolecuul 1 koolstofatoom en 4 waterstofatomen heeft.
2. Tel de covalente bindingen in één methaanmolecuul:
* Koolstof vormt vier enkele covalente bindingen met vier waterstofatomen.
3. Bereken het aantal methaanmoleculen in 8 g:
* Vind de molaire massa methaan: 12.01 g/mol (c) + 4 * 1.01 g/mol (h) =16,05 g/mol
* Bereken het aantal mol: 8 g / 16,05 g / mol =0,498 mol
* Gebruik Avogadro's nummer om het aantal moleculen te vinden: 0,498 mol * 6.022 x 10²³ Moleculen/mol ≈ 3,00 x 10²³ Moleculen
4. Bereken het totale aantal covalente obligaties:
* bindingen per molecuul: 4 bindingen/molecuul
* Totale obligaties: (3,00 x 10²³ Moleculen) * (4 bindingen/molecuul) = 1.20 x 10²⁴ Covalent bindingen
Daarom zijn er ongeveer 1,20 x 10²⁴ covalente bindingen in 8 g methaan.
 Wat zijn de effecten van antivries op het milieu?
Wat zijn de effecten van antivries op het milieu?  Een proefschrift bracht nieuwe hi-precisie massametingen voor atomaire massa's van isotopen zwaarder dan ijzer
Een proefschrift bracht nieuwe hi-precisie massametingen voor atomaire massa's van isotopen zwaarder dan ijzer Hoeveel mol fluor in 3 borontrifluoride?
Hoeveel mol fluor in 3 borontrifluoride?  Wat gebeurt er met de oplosbaarheid van calciumchloride als u oplossing koelt?
Wat gebeurt er met de oplosbaarheid van calciumchloride als u oplossing koelt?  Welke combinatie van metalen zou elektrolytische corrosie het meest uitgesproken zijn?
Welke combinatie van metalen zou elektrolytische corrosie het meest uitgesproken zijn?
 Bedrijven denken dat ze bovenop het koolstofrisico zitten, maar toeristische bestemmingen hebben nauwelijks een idee
Bedrijven denken dat ze bovenop het koolstofrisico zitten, maar toeristische bestemmingen hebben nauwelijks een idee Wetenschappers ontdekken oorzaak van Atlantische kusten zeespiegelstijging hotspots
Wetenschappers ontdekken oorzaak van Atlantische kusten zeespiegelstijging hotspots 3 eenvoudige, einde-zomer science-hacks die je nu moet proberen
3 eenvoudige, einde-zomer science-hacks die je nu moet proberen
Het is officieel - we zijn in de homestretch van de zomer. En hoewel het niet echt de tijd is om voor het nieuwe jaar te gaan studeren, is er geen reden waarom je de laatste paar weken
 Dolfijnen migreren of overwinteren?
Dolfijnen migreren of overwinteren?  Vliegtuigen en voertuigen belangrijkste boosdoeners die iconische natuurlijke geluiden maskeren in vredige nationale parken
Vliegtuigen en voertuigen belangrijkste boosdoeners die iconische natuurlijke geluiden maskeren in vredige nationale parken
Hoofdlijnen
- Wat betekent niche in de wetenschap?
- Is het levend of dood? Team laat zien hoe je de thermische handtekeningen van afzonderlijke cellen kunt meten
- Als een dier uit de voedselketen wordt verdwenen, wat is dan het effect op de keten?
- Onderzoekers ontdekken hoe dieren hun puntige lichaamsdelen laten groeien
- Nieuwe hoop voor ernstig bedreigde aap met stompe neus in Myanmar
- Bewaakt een celwand voedsel en water in cel?
- Wat heeft de Griekse wetenschapper Aristarchus ontwikkeld?
- Wat doet het endoplasmatisch reticulum?
- Mieren in het bladerdak van het Amazone-regenwoud hebben veel meer bacteriën in hun ingewanden dan grondbewoners
- Onderzoekers ontwikkelen techniek om koolstofdioxide en methaan te hergebruiken

- Pig-Pen-effect:het mengen van huidolie en ozon kan een persoonlijke vervuilingswolk veroorzaken
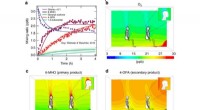
- Onderzoek naar perovskiet-silicium tandemcellen laat nieuwe weg zien

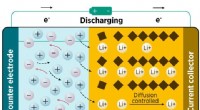
- Röntgenanalyse onthult het oplaadmechanisme van een veelbelovend elektrodemateriaal
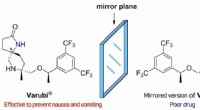
- Nuttige verbindingen synthetiseren zonder ongewenste chirale partners te vormen
 Hoe 208V te verhogen naar 230V
Hoe 208V te verhogen naar 230V  VS officieel terug in akkoord Parijs belooft klimaatactie
VS officieel terug in akkoord Parijs belooft klimaatactie Nooit eerder geziene glasschade op nanoniveau zien
Nooit eerder geziene glasschade op nanoniveau zien Wat is lasverval?
Wat is lasverval?  Nieuw apparaat belooft lagere bedrijfskosten voor de spoorsector
Nieuw apparaat belooft lagere bedrijfskosten voor de spoorsector VN:Wereldbevolking stijgt naar verwachting tot 9,7 miljard in 2050
VN:Wereldbevolking stijgt naar verwachting tot 9,7 miljard in 2050 Wat zijn de drie veel voorkomende soorten neerslagvorm?
Wat zijn de drie veel voorkomende soorten neerslagvorm?  Waarom is xenon belangrijk voor de mens?
Waarom is xenon belangrijk voor de mens?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

