
Wetenschap
Waarom roest zink niet?
Dit is de reden waarom zink Rust lijkt te weerstaan:
* zink vormt zijn eigen beschermende laag: Wanneer zink wordt blootgesteld aan lucht en vocht, ondergaat het een proces genaamd oxidatie , vergelijkbaar met roesten. In plaats van schilferige, roodbruine ijzeroxide (roest) te vormen, vormt zink echter een dunne, strak gebonden laag zinkoxide . Deze laag is dicht en niet-poreus en fungeert effectief als een barrière voor verdere corrosie.
* Galvanische bescherming: Wanneer zink wordt gebruikt als een coating op staal (galvanisatie), biedt dit galvanische bescherming . Zink is reactiever dan ijzer, wat betekent dat het eerst zal corroderen in contact met vocht. Dit creëert een offeranode die het staal beschermt tegen roesten.
* Andere factoren: De aanwezigheid van andere metalen in het milieu kan ook beïnvloeden hoe zink reageert. Zink is bijvoorbeeld eerder geneigd om te corroderen in aanwezigheid van zwaveldioxide, een veel voorkomende verontreinigende stof.
Dus, hoewel zink niet roest als ijzer, corrodeer het, op een andere manier. Het is dit unieke corrosiegedrag dat het een uitstekende beschermende coating maakt voor metalen zoals staal.
 Hoeveel mol lucht bevinden zich in een 3L -container bij 1 atm druk en 293 K?
Hoeveel mol lucht bevinden zich in een 3L -container bij 1 atm druk en 293 K?  Wanneer germanium vloeibaar is, wat is dan het vriespunt?
Wanneer germanium vloeibaar is, wat is dan het vriespunt?  Onderzoekers identificeren het afweermechanisme van eenhoorn dat bacteriën beschermt tegen antibiotica
Onderzoekers identificeren het afweermechanisme van eenhoorn dat bacteriën beschermt tegen antibiotica  Welke verbindingen zijn koolstof tetrluoride?
Welke verbindingen zijn koolstof tetrluoride?  Welke stof wordt opgebruikt tijdens fotosynthese?
Welke stof wordt opgebruikt tijdens fotosynthese?
Hoofdlijnen
- Verdeel en definieer:aanwijzingen om te begrijpen hoe stamcellen verschillende soorten produceren
- Antibiotica in actie zien in een pathogene bacterie
- Welke stoffen helpen de lichaamsfuncties te reguleren?
- Is een obligate halofiel organisme dat een hoge osmotische druk vereist?
- Wat zijn de belangrijkste onderdelen van de celcyclus?
- Waarom papegaaien soms elkaars baby's adopteren (of doden)
- Waarom is een microscoop belangrijk?
- Het visfeest is in wezen een benzinestation en trekt zeeleeuwen naar Pier 39 in aantallen die in 15 jaar niet meer zijn gezien
- De methoden van inventarisatie in Microbes
- Een grote stap voorwaarts in organische elektronica

- Titan-in-a-glass-experimenten duiden op minerale samenstelling van de Saturnusmaan

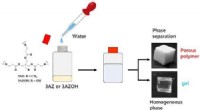
- Gewoon water toevoegen:een eenvoudige methode om veelzijdige poreuze polymeren te verkrijgen
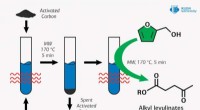
- Chemicus stelt nieuwe manier voor om de brandstofkwaliteit te verbeteren met behulp van microgolfstraling
- Nieuwe technologie verbetert de productie van waterstof

 Pentagon-chef zegt dat klimaatverandering de veiligheid bedreigt:rapport
Pentagon-chef zegt dat klimaatverandering de veiligheid bedreigt:rapport Studie laat zien hoe economische ontwikkelingsdoelen in evenwicht kunnen worden gebracht met milieubehoud met behulp van vrij beschikbare gegevens
Studie laat zien hoe economische ontwikkelingsdoelen in evenwicht kunnen worden gebracht met milieubehoud met behulp van vrij beschikbare gegevens Nieuw onderzoek beschrijft hoe ADHD ondernemers een voorsprong geeft
Nieuw onderzoek beschrijft hoe ADHD ondernemers een voorsprong geeft  Wat is het verschil tussen rode en bruine dwergsterren?
Wat is het verschil tussen rode en bruine dwergsterren?  Publiek zal meer dan $ 500 miljoen per jaar betalen voor verbeteringen in orkaanvoorspellingen, studie vondsten
Publiek zal meer dan $ 500 miljoen per jaar betalen voor verbeteringen in orkaanvoorspellingen, studie vondsten Zijn alle stollingsgesteenten gevormd in de aarde?
Zijn alle stollingsgesteenten gevormd in de aarde?  Azeotropisch mengsel van zoutzuur en water?
Azeotropisch mengsel van zoutzuur en water?  Vooruitzichten voor de poolgebieden in een 2 graden warmere wereld
Vooruitzichten voor de poolgebieden in een 2 graden warmere wereld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

