
Wetenschap
Welk type binding wordt gevormd tussen boor en waterstof?
Dit is waarom:
* elektronegativiteit: Boron heeft een elektronegativiteit van 2.0, terwijl waterstof een elektronegativiteit van 2.1 heeft. Het verschil in elektronegativiteit tussen hen is erg klein, wat betekent dat ze bijna even elektronen delen.
* delen van elektronen: In een covalente binding delen atomen elektronen om een stabiele elektronenconfiguratie te bereiken. In het geval van boor en waterstof deelt het booratoom zijn drie valentie -elektronen met drie waterstofatomen, die een molecuul vormen met de formule BH₃. Elk waterstofatoom draagt één elektron bij aan het gedeelde paar.
Hoewel het een covalente binding is, is het vermeldenswaard dat de binding in boorhydriden vaak wordt beschreven als een "bananenbinding" vanwege de ongebruikelijke structuur. Dit komt omdat het booratoom slechts 6 elektronen in zijn valentieschaal heeft, waardoor een situatie ontstaat waarin de elektronen niet ideaal gelegen zijn voor een typische covalente binding. Het resultaat is een enigszins gebogen of bananenvormige, binding.
 Is toxiciteit chemische of fysische eigenschappen?
Is toxiciteit chemische of fysische eigenschappen?  Worden substraten geconsumeerd in enzymreacties?
Worden substraten geconsumeerd in enzymreacties?  De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren
De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren Waarom is hun meer zuurstof in water nabij het oppervlak?
Waarom is hun meer zuurstof in water nabij het oppervlak?  Hoe identificeer je lead ii chloride?
Hoe identificeer je lead ii chloride?
 Video:Wat kan orkaan Irma ons vertellen over de toekomst van Atlantische orkanen?
Video:Wat kan orkaan Irma ons vertellen over de toekomst van Atlantische orkanen? NASA ziet tropische storm Cindy de Gulf Coast doordrenken
NASA ziet tropische storm Cindy de Gulf Coast doordrenken Studie:gletsjers in Azië worden geconfronteerd met enorme smelting door de opwarming van de aarde
Studie:gletsjers in Azië worden geconfronteerd met enorme smelting door de opwarming van de aarde Wat is de wetenschappelijke houding van nederigheid die het meest waarschijnlijk wordt ondermijnd?
Wat is de wetenschappelijke houding van nederigheid die het meest waarschijnlijk wordt ondermijnd?  Wat maakt een omgeving ongezond voor de organismen?
Wat maakt een omgeving ongezond voor de organismen?
Hoofdlijnen
- Wat geeft de cel vormen?
- Welke dosis classificatie betekent in de wetenschap?
- Welke wetenschapper bestudeert Flora?
- Wat beschrijft de structuur van DNA niet?
- Wat was de impact waarbij dinosauriërs omkwamen?
- De sleutel tot het kweken van natuurlijk weefsel voor de reconstructie van het vrouwelijk voortplantingssysteem ontgrendeld
- Onderzoekers identificeren een verscheidenheid aan stenen werktuigen van chimpansees voor het kraken van verschillende soorten noten
- Welke moleculen behouden de vorm die nodig is om biologisch actief te zijn vanwege intermoleculaire krachten?
- Houden ze je in de gaten? De kleine hersenen van bijen en wespen kunnen gezichten herkennen
- Ozon breekt THC af dat is afgezet op oppervlakken van derdehands cannabisrook

- Bier brouwen dat langer vers smaakt

- Nieuw PET-achtig plastic direct gemaakt van afvalbiomassa

- Oxidatie in nieuw coatingmateriaal voor gasturbinemotoren van vliegtuigen
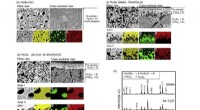
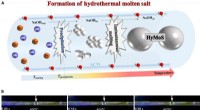
- Een nieuw oplosmiddelsysteem:Hydrothermisch gesmolten zout
 Hoe tomatenplanten hun wortels gebruiken om water te rantsoeneren tijdens droogte
Hoe tomatenplanten hun wortels gebruiken om water te rantsoeneren tijdens droogte  Buiglicht voor veiliger rijden; onzichtbaarheidsmantels op komst?
Buiglicht voor veiliger rijden; onzichtbaarheidsmantels op komst? Klimaatvriendelijke landbouwstrategieën kunnen het land verbeteren en inkomsten genereren voor boeren
Klimaatvriendelijke landbouwstrategieën kunnen het land verbeteren en inkomsten genereren voor boeren Welke gebruikelijke eenheden worden gebruikt om het volume te meten?
Welke gebruikelijke eenheden worden gebruikt om het volume te meten?  Het effect van sociale klasse op interpersoonlijke relaties
Het effect van sociale klasse op interpersoonlijke relaties Verbeterde versterkertechnologie voor gebruik in positronemissietomografie
Verbeterde versterkertechnologie voor gebruik in positronemissietomografie Zijn MXenes de toekomst van nanotechnologie?
Zijn MXenes de toekomst van nanotechnologie? Chemici ontdekken eenvoudigere methode om wondermateriaal te maken
Chemici ontdekken eenvoudigere methode om wondermateriaal te maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

