
Wetenschap
Wat zijn de obligatietypen van ICL3 N20 en licll uw keuzes zijn covalent ionisch metallic?
* icl3 (jodium trichloride) : covalent
* Jodium en chloor zijn beide niet -metalen. Covalente bindingen vormen zich tussen niet -metalen.
* Het elektronegativiteitsverschil tussen jodium en chloor is niet groot genoeg om een volledig ionische binding te creëren.
* ICL3 vertoont polaire covalente bindingen vanwege het elektronegativiteitsverschil, maar het totale molecuul is niet -polair.
* n2o (stikstofoxide) : covalent
* Stikstof en zuurstof zijn beide niet -metalen. Covalente bindingen vormen zich tussen niet -metalen.
* N2O heeft een lineaire structuur en vertoont polaire covalente bindingen.
* licl (lithiumchloride) : ionisch
* Lithium (Li) is een metaal en chloor (CL) is een niet -metaal. Ionische bindingen vormen zich tussen metalen en niet -metalen.
* Lithium verliest gemakkelijk een elektron om een positief ion te worden (Li+), terwijl chloor een elektron krijgt om een negatief ion te worden (Cl-). De elektrostatische aantrekkingskracht tussen deze tegengesteld geladen ionen creëert de ionische binding.
 Biotische factoren in ecosystemen
Biotische factoren in ecosystemen Wat is de reikwijdte van de milieuwetenschap?
Wat is de reikwijdte van de milieuwetenschap?  Hoe intensieve landbouw een wilde plant in alomtegenwoordig onkruid veranderde
Hoe intensieve landbouw een wilde plant in alomtegenwoordig onkruid veranderde  Wat is de betekenis van de natuur en de reikwijdte van het onderwijs?
Wat is de betekenis van de natuur en de reikwijdte van het onderwijs?  Wetenschappers brengen zeewaterbedreiging in kaart voor aquifers aan de centrale kust van Californië
Wetenschappers brengen zeewaterbedreiging in kaart voor aquifers aan de centrale kust van Californië
Hoofdlijnen
- Waar zijn stamcellen gevestigd?
- Wanneer een virus het cel binnenkomt?
- Waar liggen de volgende zoönotische virussen op de loer?
- Hoe een 'antibioticum' bacteriën helpt eten
- Welke cellen zou ik gebruiken om DNA van een levende persoon te extraheren?
- Onthul de geheimen van plantgezondheid en koolstofopslag met rhizosphere-on-a-chip
- Wat voor soort micro -organisme rots hout bederft voedsel en veroorzaakt huidziekten?
- Wat gebeurt er met een cel als het DNA-chromosomen niet kopieert voordat het zich splitst?
- Staat, FBI onderzoekt ziekte die ziek is, dode honden
- Nieuwe screeningsmethode ontwikkeld om te bevestigen of deuteratie de metabole stabiliteit verbetert
- Implanteerbaar piëzo-elektrisch polymeer verbetert gecontroleerde afgifte van medicijnen
- Analyse levert aanwijzingen op voor chemische samenstelling, natuurlijke veroudering van 100 jaar oud bier

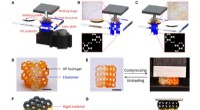
- 3D-printen van zeer rekbare hydrogel met diverse UV-uithardbare polymeren
- Onderzoekers ontwikkelen snellere test voor cannabiskwaliteit

 De zoete smaak van onzekerheid:winnaars wachten graag tot ze ontdekken wat ze hebben gewonnen
De zoete smaak van onzekerheid:winnaars wachten graag tot ze ontdekken wat ze hebben gewonnen  Laser van geluid belooft uiterst kleine fenomenen te meten
Laser van geluid belooft uiterst kleine fenomenen te meten Bestudeer details waarom 2D-vorming van molybdeendisulfide een snelheidsboost krijgt van zout
Bestudeer details waarom 2D-vorming van molybdeendisulfide een snelheidsboost krijgt van zout Nieuw milieudetectie- en monitoringsysteem getest en geëvalueerd
Nieuw milieudetectie- en monitoringsysteem getest en geëvalueerd Zijn er verborgen kosten bij het gebruik van geothermische energie?
Zijn er verborgen kosten bij het gebruik van geothermische energie?  Wat is het geologische proces?
Wat is het geologische proces?  Welke planeten orbitale snelheid is dertig kilometer per seconde?
Welke planeten orbitale snelheid is dertig kilometer per seconde?  Hoe grote vlaktes zien eruit?
Hoe grote vlaktes zien eruit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

