
Wetenschap
Wat is de structurele formule voor stikstofdioxide?
o =n-o
Verklaring:
* stikstof (n) is het centrale atoom en heeft in totaal 5 valentie -elektronen.
* zuurstof (O) heeft elk 6 valentie -elektronen.
* Dubbele binding: Eén zuurstofatoom vormt een dubbele binding met het stikstofatoom.
* enkele binding: Het andere zuurstofatoom vormt een enkele binding met het stikstofatoom.
* eenzame paren: Elk zuurstofatoom heeft twee eenzame paren elektronen.
Deze structuur voldoet aan de octetregel voor alle atomen, wat betekent dat elk atoom 8 elektronen in zijn buitenste schaal heeft.
Het is belangrijk op te merken dat de structuur eigenlijk een resonantiehybride is, wat betekent dat de dubbele binding kan worden weergegeven tussen beide zuurstofatoom. Dit geeft het molecuul een symmetrische structuur met een bindingsorder van 1,5 voor elke N-O-binding.
 Hexamere lanthanide-organische capsules met tertiaire structuur, opkomende functies
Hexamere lanthanide-organische capsules met tertiaire structuur, opkomende functies Hoeveel atomen zijn er in NAHSO4?
Hoeveel atomen zijn er in NAHSO4?  Welk reagens dat de chemische eigenschappen van Ag en Mg onderscheidt?
Welk reagens dat de chemische eigenschappen van Ag en Mg onderscheidt?  Heeft CACL2 een hooggeleidingswaarde wanneer opgelost in gedestilleerd water?
Heeft CACL2 een hooggeleidingswaarde wanneer opgelost in gedestilleerd water?  Is c2h8 een elektrolyt-propaangas dat wordt gebruikt in barbecuetanks?
Is c2h8 een elektrolyt-propaangas dat wordt gebruikt in barbecuetanks?
 EU-huishoudens verspillen meer dan 17 miljard kg verse groenten en fruit per jaar
EU-huishoudens verspillen meer dan 17 miljard kg verse groenten en fruit per jaar Wat de dood van een eenzame inheemse man in Brazilië ons kan vertellen over onze wereldwijde toekomst
Wat de dood van een eenzame inheemse man in Brazilië ons kan vertellen over onze wereldwijde toekomst Steden en hun toenemende impact op de biodiversiteit - een globaal overzicht
Steden en hun toenemende impact op de biodiversiteit - een globaal overzicht Wat is de sfeer in de kunst?
Wat is de sfeer in de kunst?  Wat zijn enkele positieve effecten van een orkaan?
Wat zijn enkele positieve effecten van een orkaan?
Hoofdlijnen
- Hoeveel chromatiden zijn aanwezig in een chromosoom T het begin van mitose?
- Wat zijn de gemeenschappelijke eigenschappen van de wetenschappers?
- Wat zijn de eigenschappen van kunststof biopol?
- Wat is koesteren?
- Wanneer twee cellen met N -aantal chromosomen fuseren, welk type cel resulteren?
- Wat is een manier die wetenschapper hypothesen genereert?
- Welke term wordt gebruikt om een chipmunk te beschrijven dat zaden of fruit eet?
- Hoe zit het met organismen is dat taxonomische sleutels kunnen worden gebruikt om te helpen bepalen?
- Wat begrijpt u bij termijnonderzoek?
- Selectieve fotothermische therapie met supramoleculaire radicale anionen die in situ worden gegenereerd
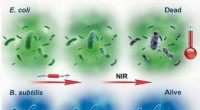
- Oplossing voor fout in synchrotron-onderzoek kan de resultaten verbeteren

- Onderzoekers onderzoeken enzymen die een kation gebruiken, geen zuurstoftoevoeging, om reacties te stimuleren
- Kanker op ground zero aanpakken met designer moleculen

- Biochemische superlijm opent nieuwe benadering van vaccinontwikkeling
 Wat betekent classificeren in de wetenschap?
Wat betekent classificeren in de wetenschap?  Windparken efficiënter maken
Windparken efficiënter maken Wat is een eenvoudige truss
Wat is een eenvoudige truss  Wat is het proces waar stukjes rots in stromen kleiner en ronder worden?
Wat is het proces waar stukjes rots in stromen kleiner en ronder worden?  Wat voor soort stof is geleidend wanneer opgelost in water?
Wat voor soort stof is geleidend wanneer opgelost in water?  Hoe zijn de wet van conservatie -energie en massa vergelijkbaar?
Hoe zijn de wet van conservatie -energie en massa vergelijkbaar?  Celestial Sphere wordt hoe in de lucht genoemd?
Celestial Sphere wordt hoe in de lucht genoemd?  Welke snelheid is Radio 4?
Welke snelheid is Radio 4?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

