
Wetenschap
Hoe atomen van verschillende elementen verschillen in hun atoomstructuur?
1. Aantal protonen (atoomnummer):
* Het meest fundamentele verschil is het aantal protonen in de kern. Dit nummer wordt het atoomnummer genoemd en het definieert het element.
* Alle waterstofatomen hebben bijvoorbeeld 1 proton, alle koolstofatomen hebben 6 protonen en alle zuurstofatomen hebben 8 protonen.
* Het aantal protonen wijzigen verandert het element volledig.
2. Aantal neutronen (atomaire massa):
* Hoewel het aantal protonen constant is voor een bepaald element, kan het aantal neutronen variëren. Deze variatie leidt tot isotopen , die atomen van hetzelfde element zijn met verschillende massa's.
* Bijvoorbeeld, koolstof-12 heeft 6 protonen en 6 neutronen, terwijl koolstof-14 6 protonen en 8 neutronen heeft.
* Verschillende isotopen van hetzelfde element hebben dezelfde chemische eigenschappen maar verschillende fysische eigenschappen vanwege hun massaverschil.
3. Aantal elektronen (elektronische configuratie):
* Het aantal elektronen in een atoom is meestal gelijk aan het aantal protonen, het handhaven van elektrische neutraliteit.
* De elektronen zijn gerangschikt in specifieke energieniveaus (schalen) en subles (orbitalen) rond de kern. Deze opstelling wordt de elektronische configuratie genoemd .
* De elektronische configuratie bepaalt de chemische eigenschappen van het atoom, zoals zijn reactiviteit en de soorten bindingen die het kan vormen.
Samenvattend:
* Atomisch nummer Definieert het element en bepaalt het aantal protonen.
* atomaire massa wordt beïnvloed door het aantal neutronen en kan variëren binnen een element.
* Elektronische configuratie Bepaalt het chemische gedrag van een element door de opstelling van elektronen te beschrijven.
Deze verschillen in atoomstructuur verklaren waarom elementen verschillende eigenschappen hebben en zich anders gedragen in chemische reacties.
Hoofdlijnen
- Welk deel van de bloem waar eten wordt opgeslagen als zetmeel?
- Hoe bavianen gezonde gezinsgrenzen bewaren
- Wat absorberen de cel schadelijke bacteriën en andere vreemde voorwerpen?
- Wolf die verband houdt met het doden van vee zou zich kunnen voortplanten, zeggen natuurbeschermers
- Welke wordt gevonden in zowel RNA als DNA?
- Biobrandstoffen als invasieve soort?
- Epigenetica legt uit waarom je DNA je lot niet voorspelt
- Wat kikkerverkering ons kan vertellen over menselijke praatjes
- Morfologisch en biochemisch bewijs vergelijken ter ondersteuning van evolutie?
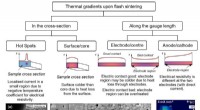
- Solid-state batterijen kunnen schoner worden gemaakt door flash-sintering op te schalen
- Wetenschappers lossen ruwe olie op in water om de samenstelling ervan te bestuderen

- Gepersonaliseerde zweetsensor meet betrouwbaar de bloedglucose zonder vingerprikken

- Goedkoop, schaalbare watersplitsing voedt de toekomstige waterstofeconomie

- Wetenschappers ontdekken snellere manier om vasculaire materialen te vervaardigen

 Hoe breek je nieuwe records op de 200 meter?
Hoe breek je nieuwe records op de 200 meter? Waarom hebben eencellige organismen geen complexe structuren nodig voor gasuitwisseling?
Waarom hebben eencellige organismen geen complexe structuren nodig voor gasuitwisseling?  Buitenaardse vorm van heet,
Buitenaardse vorm van heet,  Kunnen membranen met omgekeerde polariteit zichzelf assembleren op Saturnusmaan Titan?
Kunnen membranen met omgekeerde polariteit zichzelf assembleren op Saturnusmaan Titan? Hoe heeft de studie van zeebodem de theorie -plaattektoniek geholpen?
Hoe heeft de studie van zeebodem de theorie -plaattektoniek geholpen?  Kunnen we geen elektriciteit meer hebben?
Kunnen we geen elektriciteit meer hebben?  Wat is Safranin -oplossing in de wetenschap?
Wat is Safranin -oplossing in de wetenschap?  Wat heeft een hoger viscositeit water of sprankelend water?
Wat heeft een hoger viscositeit water of sprankelend water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


