
Wetenschap
Is kaliumatoom en een fluor is covalent of ionische binding?
* elektronegativiteit: Fluor is het meest elektronegatieve element, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen. Kalium daarentegen is een metaal en heeft een lage elektronegativiteit. Dit grote verschil in elektronegativiteit is cruciaal voor ionische binding.
* elektronenoverdracht: Wanneer kalium en fluor reageren, verliest kalium gemakkelijk zijn enkele valentie -elektron om een positief geladen kaliumion (k+) te worden. Fluorin krijgt dit elektron om een negatief geladen fluoride-ion te worden (F-).
* Elektrostatische aantrekkingskracht: De tegengesteld geladen ionen trekken elkaar sterk aan en vormen een ionische binding. Deze aantrekkingskracht resulteert in de vorming van de samengestelde kaliumfluoride (KF).
Samenvattend: Het significante verschil in elektronegativiteit tussen kalium en fluor leidt tot de overdracht van elektronen, waardoor ionen worden gevormd die elkaar aantrekken door elektrostatische krachten, wat resulteert in een ionische binding.
 Aardbevingen op de bovenste plaat veroorzaakten opwaartse kracht langs de noordelijke Hikurangi-marge in Nieuw-Zeeland
Aardbevingen op de bovenste plaat veroorzaakten opwaartse kracht langs de noordelijke Hikurangi-marge in Nieuw-Zeeland Hoe visie werkt
Hoe visie werkt  In de strijd om koraalriffen te beschermen tegen opwarmende oceanen, Amerikaanse en Australische experts bundelen hun krachten
In de strijd om koraalriffen te beschermen tegen opwarmende oceanen, Amerikaanse en Australische experts bundelen hun krachten Klimaatcrisis op een laag pitje nu pandemische dreiging opdoemt
Klimaatcrisis op een laag pitje nu pandemische dreiging opdoemt Invasieve tropische plant kan metaalverontreinigende stoffen volledig uit de Britse rivieren verwijderen - nieuwe studie
Invasieve tropische plant kan metaalverontreinigende stoffen volledig uit de Britse rivieren verwijderen - nieuwe studie
Hoofdlijnen
- Wat is het xylom en Phoelom?
- Waarom sommige uitwerpselen drijven en andere zinken
- Wetenschappers passen CRISPR aan om diabetes epigenetisch te behandelen, nierziekte, spierdystrofie
- Universeel klemeiwit stabiliseert gevouwen eiwitten:nieuw inzicht in hoe de chaperonne Hsp70 werkt
- Nieuw onderzoek naar speurhonden kan levens redden
- Wat is de betekenis van boerderijdierenaandoeningen?
- Waarom wordt DNA gesneden voordat het in een gel wordt gestopt?
- Op welke manier gebruiken cellen in ons lichaam lipiden?
- Wat zijn de drie belangrijkste koninkrijken van eukaryotisch?
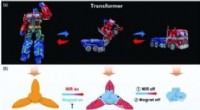
- Magnetisch gestuurd, op hydrogel gebaseerde slimme transformatoren
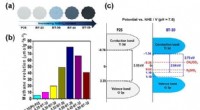
- Zeer efficiënte fotokatalysator die koolstofdioxide omzet in methaan
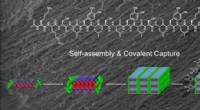
- Chemici ontwikkelen hydrogelsnaren met behulp van verbindingen die in zeedieren worden gevonden
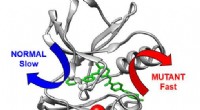
- Computersimulaties van eiwitten helpen te ontrafelen waarom resistentie tegen chemotherapie optreedt
- Nieuwe route naar moleculaire draden geschikt voor gebruik in miniatuurelektronica
 Inzicht in voetbalgeweld kan helpen bij de strijd tegen terreur
Inzicht in voetbalgeweld kan helpen bij de strijd tegen terreur De helft van de mangrove-ecosystemen in gevaar:natuurbeschermers
De helft van de mangrove-ecosystemen in gevaar:natuurbeschermers  Een laboratoriuminstrument dat u gebruikte om massa en gewicht te meten?
Een laboratoriuminstrument dat u gebruikte om massa en gewicht te meten?  Omhulsels van griepvirussen kunnen de afgifte van mRNA in cellen verbeteren
Omhulsels van griepvirussen kunnen de afgifte van mRNA in cellen verbeteren  Wie zijn zes mensen die bijdragen hebben geleverd op het gebied van genetica?
Wie zijn zes mensen die bijdragen hebben geleverd op het gebied van genetica?  Kan koffie bescherming bieden tegen besmetting met COVID-19?
Kan koffie bescherming bieden tegen besmetting met COVID-19?  Nieuw partnerschap helpt duurzame groei met aardobservaties
Nieuw partnerschap helpt duurzame groei met aardobservaties Zal 60 Watt Bulb hetzelfde wattage uitzetten op 50 en Hz?
Zal 60 Watt Bulb hetzelfde wattage uitzetten op 50 en Hz?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

