
Wetenschap
Hoeveel waterstofatomen zijn er in 3,90 mol ammoniumsulfide?
1. Begrijp de formule
Ammoniumsulfide heeft de formule (NH₄) ₂S. Dit betekent dat elk molecuul bevat:
* 2 stikstofatomen (n)
* 8 waterstofatomen (h)
* 1 zwavelatoom (s)
2. Gebruik het nummer van Avogadro
Het nummer van Avogadro vertelt ons dat er 6.022 x 10²³ deeltjes (atomen, moleculen, enz.) In één mol van een stof zijn.
3. Bereken het aantal waterstofatomen
* mol waterstofatomen: Omdat elk ammoniumsulfidemolecuul 8 waterstofatomen heeft, bevat 3,90 mol ammoniumsulfide 3,90 mol * 8 =31,2 mol waterstofatomen.
* Aantal waterstofatomen: Vermenigvuldig de mol waterstofatomen met het nummer van Avogadro:31.2 mol * 6.022 x 10²³ Atomen/mol ≈ 1,88 x 10²⁵ waterstofatomen
Daarom zijn er ongeveer 1,88 x 10²⁵ waterstofatomen in 3,90 mol ammoniumsulfide.
 Wie zegt dat dingen in de aarde vallen vanwege de zwaartekracht?
Wie zegt dat dingen in de aarde vallen vanwege de zwaartekracht?  Veterinair toxicoloog waarschuwt voor blauwalgen gevaren voor vee, huisdieren
Veterinair toxicoloog waarschuwt voor blauwalgen gevaren voor vee, huisdieren Uit nieuw onderzoek blijkt dat baby's op weg naar school meer worden blootgesteld aan schadelijke vervuiling dan op weg naar huis
Uit nieuw onderzoek blijkt dat baby's op weg naar school meer worden blootgesteld aan schadelijke vervuiling dan op weg naar huis Wat veroorzaakt seizoenen en klimaatzones?
Wat veroorzaakt seizoenen en klimaatzones?  Waarom is het woord natuurlijk een bijvoeglijk naamwoord?
Waarom is het woord natuurlijk een bijvoeglijk naamwoord?
Hoofdlijnen
- Waarom gebruikte Mendel pure broodplanten?
- Kan biochar helpen broeikasgassen te onderdrukken?
- Vijf soorten aseksuele reproductie
- Hoe weet het lichaam hoe hij mRNA moet produceren?
- Wat betekent ion?
- Waarom denk je dat cellen zo gespecialiseerd en complex zijn in plantendieren?
- Wat is het belangrijkste als je een wetenschapper bent?
- Wetenschappers onderzoeken hoe sociale netwerken gedrag beïnvloeden
- Wat is het gevolg van het invoegen van buitenlands DNA in een organisme om een nieuwe gencombinatie te produceren?
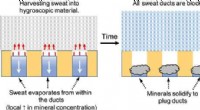
- Het zweet tegen zichzelf keren met een metaalvrije anti-transpirant
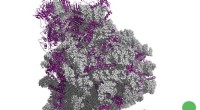
- Hoe een biofysische simulatiemethode het ontdekken van medicijndoelen kan versnellen?
- Compressief scheren kan het leven op andere planeten doen ontstaan

- Koolmonoxide verandert onder omgevingsdruk in groot defectloos grafeenkristal

- Nieuwe test biedt nauwkeurige meting van DNA-schade door chemische verbindingen

 Kunnen kwantumzwaartekrachtmodellen die voortkomen uit holografie de kosmologische versnelling verklaren?
Kunnen kwantumzwaartekrachtmodellen die voortkomen uit holografie de kosmologische versnelling verklaren?  Wat is de differentiële rotatie van de Suns?
Wat is de differentiële rotatie van de Suns?  Wordt energie toegepast om trillingen te veroorzaken in de vorm van luchtdruk een stokboog of elektriciteit?
Wordt energie toegepast om trillingen te veroorzaken in de vorm van luchtdruk een stokboog of elektriciteit?  Video:Ruimtepakontwerp van de volgende generatie
Video:Ruimtepakontwerp van de volgende generatie Welke metalen samenstelling is groen en onoplosbaar?
Welke metalen samenstelling is groen en onoplosbaar?  Kleurveranderende verbanden detecteren en behandelen bacteriële infecties
Kleurveranderende verbanden detecteren en behandelen bacteriële infecties Hoe ontdekten wetenschappers dat stenen verder weg van de heuvelrug van het midden van de oceaan ouder waren dan die in de buurt?
Hoe ontdekten wetenschappers dat stenen verder weg van de heuvelrug van het midden van de oceaan ouder waren dan die in de buurt?  Wat hebben fossielen te maken met Wegeners-theorie?
Wat hebben fossielen te maken met Wegeners-theorie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

