
Wetenschap
Wat gebeurt er als waterige broom wordt toegevoegd aan natriumchloride?
* Bromine is minder reactief dan chloor: Chloor is een sterker oxidatiemiddel dan broom. Dit betekent dat chloor een grotere neiging heeft om elektronen te winnen en te worden verminderd.
* De halogenen volgen de trend van afnemende reactiviteit langs de groep: Fluor is het meest reactief, gevolgd door chloor, broom en jodium.
* Geen verplaatsingsreactie: Om een reactie te laten optreden, zou Bromine chloor van NaCl moeten verplaatsen. Broom is echter minder reactief en kan chloor niet verplaatsen.
Daarom blijft het mengsel als afzonderlijke waterige oplossingen van broom- en natriumchloride.
Mogelijke observatie: De oplossing zal waarschijnlijk een geelbruine kleur hebben vanwege de aanwezigheid van broom.
Opmerking: Hoewel er geen significante reactie optreedt, zou als u de oplossing zou blootstellen aan zonlicht of UV -licht, een kleine hoeveelheid chloorgas kunnen worden geproduceerd. Dit komt omdat zonlicht voldoende energie kan bieden om de energiebarrière te overwinnen om een reactie te laten plaatsvinden. Deze reactie is echter erg traag en zal waarschijnlijk niet merkbaar zijn onder normale omstandigheden.
 Wat hebben zowel een atoom als een element gemeen?
Wat hebben zowel een atoom als een element gemeen?  Hoe helpt Spectroscopy elementen te identificeren?
Hoe helpt Spectroscopy elementen te identificeren?  Wat is het verschil tussen waterstofperoxide en dioxide?
Wat is het verschil tussen waterstofperoxide en dioxide?  Wat gebeurt er als kopersulfaat- en natriumhydroxidegevoel?
Wat gebeurt er als kopersulfaat- en natriumhydroxidegevoel?  Nanodeeltjessensor kan onderscheid maken tussen virale en bacteriële longontsteking
Nanodeeltjessensor kan onderscheid maken tussen virale en bacteriële longontsteking
 Hoe het water en rioolwater onder je voeten je huis kunnen overstromen (en wat je eraan kunt doen)
Hoe het water en rioolwater onder je voeten je huis kunnen overstromen (en wat je eraan kunt doen) Wat is het materiaal in de natuur dat nog nooit heeft geleefd?
Wat is het materiaal in de natuur dat nog nooit heeft geleefd?  Wat is iets dat van de aarde komt, behalve de planten of dier van de nee?
Wat is iets dat van de aarde komt, behalve de planten of dier van de nee?  Schadelijke gevolgen van de Groene Revolutie
Schadelijke gevolgen van de Groene Revolutie Smeltend ijs kan de vorm van Arctische rivierdelta's veranderen
Smeltend ijs kan de vorm van Arctische rivierdelta's veranderen
Hoofdlijnen
- De ziekte is gemakkelijker te verspreiden in de samenleving?
- Melk drinken:in onze genen?
- Welke rol speelt water in de voedselproductie van planten?
- Wanneer ontwikkelt resistentie tegen toxines zich bij dieren?
- Hoe orbitale diagrammen te doen
- Reproduceert Plant hun eigen soort?
- Waarom moeten de mitochondriën veel cristae hebben met betrekking tot fietsen of enz.?
- Hoe krijgen mensen zuurstof in hun lichaam?
- Waarom hebben wetenschappers een gemeenschappelijk meetsysteem nodig?
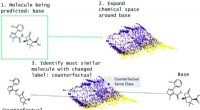
- Contrafeiten gebruiken om voorspellingen over de veiligheid van geneesmiddelen te verifiëren
- Efficiënte elektrokatalytische reductie van nitraat tot stikstof:veelbelovende manier om stikstof uit water te verwijderen

- Een strategie voor het ontwerpen van elektrolyten voor het maken van batterijen van tweewaardig metaal

- Wanneer het veranderen van één atoom moleculen beter maakt

- Veilige oplossing om olievlekken op te ruimen

 Verschillende natuurwaarden kunnen nog steeds leiden tot gezamenlijke doelstellingen voor duurzaamheid
Verschillende natuurwaarden kunnen nog steeds leiden tot gezamenlijke doelstellingen voor duurzaamheid  Wat is metaalafzetting?
Wat is metaalafzetting?  Wat u moet weten over de MyShake-app, het waarschuwingssysteem voor aardbevingen in Californië
Wat u moet weten over de MyShake-app, het waarschuwingssysteem voor aardbevingen in Californië  Geluidsgolven draaien druppels om zich te concentreren, afzonderlijke nanodeeltjes
Geluidsgolven draaien druppels om zich te concentreren, afzonderlijke nanodeeltjes De effecten van smeltende gletsjers op tropische gemeenschappen
De effecten van smeltende gletsjers op tropische gemeenschappen Wat is het verschil tussen de manier waarop twee elektronentransportshuttles (NADH en FADH2) elektronen in de keten afgeven?
Wat is het verschil tussen de manier waarop twee elektronentransportshuttles (NADH en FADH2) elektronen in de keten afgeven?  Radioactiviteit van olie- en gasafvalwater blijft bestaan in stroomsedimenten in Pennsylvania
Radioactiviteit van olie- en gasafvalwater blijft bestaan in stroomsedimenten in Pennsylvania Wat voor soort rotstypes zijn te vinden op hotspots?
Wat voor soort rotstypes zijn te vinden op hotspots?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

