
Wetenschap
Maakt ijzer en natriumchloride een verplaatsingsreactie?
* Activiteitenreeks: IJzer is minder reactief dan natrium. De activiteitenreeks van metalen rangschikt ze in volgorde van hun reactiviteit. Een meer reactief metaal kan een minder reactief metaal uit de verbinding verplaatsen.
* Reactievoorspelling: In dit geval, als er een verplaatsingsreactie zou optreden, zouden we verwachten dat ijzer natrium uit natriumchloride verplaatst, waardoor ijzerchloride (Fecl₂) en natrium wordt gevormd. Deze reactie vindt echter niet plaats onder normale omstandigheden.
Waarom het niet gebeurt:
* stabiliteit: Natriumchloride (NaCl) is een zeer stabiele verbinding. De binding tussen natrium en chloor is sterk.
* Energieoverwegingen: De reactie om natrium te verplaatsen uit natriumchloride vereist een aanzienlijke hoeveelheid energie om de stabiliteit van de bestaande binding te overwinnen. Het is onwaarschijnlijk dat deze energie -input onder normale omstandigheden wordt verstrekt.
Conclusie:
Hoewel ijzer en natriumchloride beide veel voorkomende stoffen zijn, reageren ze niet gemakkelijk om een verplaatsingsreactie te vormen. Het verschil in hun reactiviteit, zoals bepaald door de activiteitenreeks, voorkomt dat dit gebeurt.
 Wat betekent het concept van ruimtelijke interactie?
Wat betekent het concept van ruimtelijke interactie?  Granieten kunnen het raadsel van het lokaliseren van metalen oplossen die cruciaal zijn voor koolstofarme technologie
Granieten kunnen het raadsel van het lokaliseren van metalen oplossen die cruciaal zijn voor koolstofarme technologie Wat is het Coldist Biome op aarde?
Wat is het Coldist Biome op aarde?  Wat is de beschrijving van het behoud?
Wat is de beschrijving van het behoud?  Welke keuzes worden gedefinieerd als de primaire lens waardoor leden van een cultuur worden geobserveerd en sense wereld is?
Welke keuzes worden gedefinieerd als de primaire lens waardoor leden van een cultuur worden geobserveerd en sense wereld is?
Hoofdlijnen
- Enzymen in lysosomen verteren organen waarom?
- Hoe zijn enzymen gerelateerd aan macromoleculen en chemische reacties?
- Welke kenmerken maken eiwitten de meest veelzijdige macromoleculen in cellen termen van functionele mogelijkheden?
- Vriend of vijand? Onderzoekers onderzoeken de mysterieuze microben die in koralen leven
- Hittegolf veroorzaakt valse herfst in het VK
- Waarom is het belangrijk dat RNA kleiner is dan DNA?
- Onderzoekers:Hoe authenticeer je je niet-menselijke cellijnen?
- Een betere pinda op je bord? Nieuwe bevindingen onthullen potentieel voor gewasverbetering
- Hoe heet het wanneer een bacterie virus gebruikt om zijn andere DNA een andere bacterie over te dragen?
- Onderzoekers ontdekken dat ruimte tussen polymeerketens de energieconversie beïnvloedt

- Hoe geleidende gels te laten kleven als ze nat zijn?

- Ontsmetten van amandelen en noten met gecomprimeerde kooldioxide

- Video:De ruimtevaartkracht van... plassen?

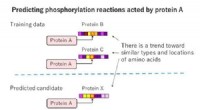
- Fujitsu ontwikkelt technologie om biochemische reacties te voorspellen, opheldering van de mechanismen van genetische aandoeningen
 Wat is het verschil tussen endotherme en exotherme verandering?
Wat is het verschil tussen endotherme en exotherme verandering?  Hoe kan ik de huidige maanfase controleren?
Hoe kan ik de huidige maanfase controleren?  In plaats van studenten richting ondernemerschap te duwen, ze moeten geholpen worden met het begrijpen van persoonlijke prioriteiten
In plaats van studenten richting ondernemerschap te duwen, ze moeten geholpen worden met het begrijpen van persoonlijke prioriteiten Het hebben van werknemers in het buitenland helpt bedrijven om Amerikaanse belastingvoordelen te behalen
Het hebben van werknemers in het buitenland helpt bedrijven om Amerikaanse belastingvoordelen te behalen Welke veranderingen hebben plaatsgevonden in het naaldbos?
Welke veranderingen hebben plaatsgevonden in het naaldbos?  Internet naar TLS 1.3:waar ben je mijn hele leven geweest
Internet naar TLS 1.3:waar ben je mijn hele leven geweest In welke fysieke toestand wordt 10 grammen broom de meeste thermische energie opslaan?
In welke fysieke toestand wordt 10 grammen broom de meeste thermische energie opslaan?  Hoe jetpacks werken
Hoe jetpacks werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

