
Wetenschap
Welk type binding wordt gevormd tussen stikstof en broom?
Dit is waarom:
* elektronegativiteit: Stikstof (N) heeft een elektronegativiteit van 3,04, terwijl broom (BR) een elektronegativiteit van 2,96 heeft. Het verschil in elektronegativiteit is niet groot genoeg om een ionische binding te creëren.
* Elektronen delen: Zowel stikstof als broom moeten elektronen krijgen om een stabiele octetconfiguratie te bereiken. Ze bereiken dit door elektronen te delen en een covalente binding te vormen.
Het specifieke type covalente binding is polaire covalent . Dit komt omdat, hoewel het verschil van elektronegativiteit klein is, het niet nul is. Dit betekent dat de gedeelde elektronen iets meer tijd doorbrengen dichter bij het stikstofatoom, waardoor de stikstof enigszins negatief is en de broom enigszins positief.
 Kunnen kritieke metalen voor hernieuwbare energieproducten worden gevonden in bestaande mijnen? Nieuw onderzoek zegt ja
Kunnen kritieke metalen voor hernieuwbare energieproducten worden gevonden in bestaande mijnen? Nieuw onderzoek zegt ja Is de natuur vooral een knutselaar of een uitvinder?
Is de natuur vooral een knutselaar of een uitvinder?  Positieve feedback tussen Oost-Aziatische circulatie op de middelste breedtegraden en de temperatuur van het landoppervlak
Positieve feedback tussen Oost-Aziatische circulatie op de middelste breedtegraden en de temperatuur van het landoppervlak Grace komt aan land in Mexico als grote orkaan
Grace komt aan land in Mexico als grote orkaan Loodvervuiling door indianen toegeschreven aan verpletterende galena voor glitterverf
Loodvervuiling door indianen toegeschreven aan verpletterende galena voor glitterverf
Hoofdlijnen
- Waar komen grondstoffen vandaan in planten?
- Wat hebben rommelige gazons te maken met bijenvoer? Een deskundige legt het uit
- Studie wijst op cellulaire respons op druk in zeester-embryo's
- Het reuzenschaap dat Tadzjikistan helpt de klimaatverandering te doorstaan
- Wat is ureum?
- Wat is de studie van ethische implicaties Biologisch onderzoek en toepassingen, vooral in veldgeneeskunde?
- Hoe doden mensen bacteriën in hun lichaam?
- Wat is de taak van klieren in het mannelijke reproductieve systeem?
- Wetenschappers laten zien hoe het energielandschapsalgoritme de interfasedynamiek van DNA detailleert
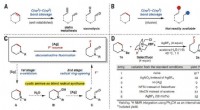
- Zilverzout dat wordt gebruikt om C-C-bindingen in ongespannen cyclische aminen te verbreken
- Zeer efficiënte waterstofgasproductie met behulp van zonlicht, water en hematiet

- Kameleonachtig materiaal verrijkt met boor komt dichter bij het nabootsen van hersencellen

- Hoe enzymen waterstof produceren

- Water vormt ruggengraat van hydratatie rond DNA, groepsvondsten

 Welke energietransformatie vindt plaats in de kern van een kernreactor?
Welke energietransformatie vindt plaats in de kern van een kernreactor?  Onderzoek werpt nieuw licht op krachten die gevoelige kustlijnen bedreigen
Onderzoek werpt nieuw licht op krachten die gevoelige kustlijnen bedreigen Een team heeft onderzocht wat de motivatie was voor het gebruik van sociale media tijdens het evenement van 6 januari
Een team heeft onderzocht wat de motivatie was voor het gebruik van sociale media tijdens het evenement van 6 januari Wat kan een organisme doen tijdens het leven in het organisme?
Wat kan een organisme doen tijdens het leven in het organisme?  Wetenschappelijk wat strekt zich uit van horizon tot horizon?
Wetenschappelijk wat strekt zich uit van horizon tot horizon?  Wat is het laadonderzoek naar voorspelling van energievereiste?
Wat is het laadonderzoek naar voorspelling van energievereiste?  Facebook neemt hooggeplaatste advocaat van het Amerikaanse ministerie van Buitenlandse Zaken in dienst
Facebook neemt hooggeplaatste advocaat van het Amerikaanse ministerie van Buitenlandse Zaken in dienst Wanneer landden ons voor het eerst op de maan?
Wanneer landden ons voor het eerst op de maan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

