
Wetenschap
Hoeveel moleculen broom zijn aanwezig in 120 gram gas?
1. Bepaal de molaire massa broom:
* Bromine bestaat als een diatomee molecuul (Br₂).
* De atoommassa van broom (BR) is ongeveer 79,90 g/mol.
* De molaire massa van Br₂ is 2 * 79,90 g/mol =159,80 g/mol.
2. Bereken het aantal mol:
* Mol =massa / molaire massa
* Mol =120 g / 159,80 g / mol
* Mol ≈ 0,75 mol
3. Gebruik het nummer van Avogadro:
* Het nummer van Avogadro stelt dat er 6.022 x 10²³ moleculen in één mol van elke stof zijn.
* Aantal moleculen =mollen * Avogadro's nummer
* Aantal moleculen ≈ 0,75 mol * 6.022 x 10²³ Moleculen/mol
* Aantal moleculen ≈ 4.52 x 10²³ Moleculen
Daarom zijn er ongeveer 4,52 x 10²³ broommoleculen aanwezig in 120 gram broomgas.
 Ingenieurs pionieren met het vormingsproces van platinagranaten, eerste waarneming ooit bereiken
Ingenieurs pionieren met het vormingsproces van platinagranaten, eerste waarneming ooit bereiken Welk element deelt de meeste kenmerken met koolstof?
Welk element deelt de meeste kenmerken met koolstof?  Schrijf met warmte, afkoelen en herhaal dan met herschrijfbaar papier
Schrijf met warmte, afkoelen en herhaal dan met herschrijfbaar papier Wat is de brandstofbron die wordt gebruikt voor glycolyse?
Wat is de brandstofbron die wordt gebruikt voor glycolyse?  Wat betekent in chemische tankers één voetmonster?
Wat betekent in chemische tankers één voetmonster?
Hoofdlijnen
- Britse rundvleesboeren willen overstappen naar netto nul, maar praktische en financiële belemmeringen staan in de weg
- Wat is het proces waar gist koolstofdioxide produceert?
- Vlezige structuur rondom het zaad in een angiosperm?
- Wat weten we werkelijk over de geschiedenis van het gebruik van biologische wapens?
- Welk twee lichaamssysteem is het meest zichtbaar in Ascaris?
- Geef de fasen in het proces van bevruchtingszoogdieren?
- Waarom wordt colchicine gebruikt voor het bereiden van een metafasespread?
- Welk enzym verteert eiwit?
- Wat is de vorm van mRNA?
- Hoe goede darmbacteriën het risico op hartaandoeningen helpen verminderen

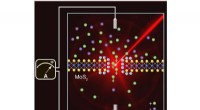
- Elektriciteit opwekken in estuaria met licht en osmose
- Forensisch onderzoek bewijst dat textielvezels kunnen worden overgedragen tussen kleding zonder contact

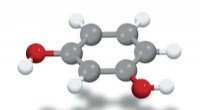
- Selectieve synthese van meta-isomeren nu mogelijk
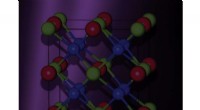
- Nieuwe katalysatoren maken van unieke metaallegeringen
 Hoe sterk geseksualiseerde beelden invloed hebben op Instagram - en hoe intimidatie wijdverbreid is
Hoe sterk geseksualiseerde beelden invloed hebben op Instagram - en hoe intimidatie wijdverbreid is Wat ontdekte James Joule over elektriciteit?
Wat ontdekte James Joule over elektriciteit?  Wat is de K-Shell-bindende energie voor Rhodium?
Wat is de K-Shell-bindende energie voor Rhodium?  Wat weegt 1 keizerlijke gallon van Avgas?
Wat weegt 1 keizerlijke gallon van Avgas?  Is koperchloride een ionische verbinding?
Is koperchloride een ionische verbinding?  Wie is het meetapparaat uitgevonden?
Wie is het meetapparaat uitgevonden?  Misschien kun je te dun zijn? Maak kennis met 's werelds dunste wolkenkrabber
Misschien kun je te dun zijn? Maak kennis met 's werelds dunste wolkenkrabber  Een nieuwe manier vinden om sepsis in een laat stadium te bestrijden door de antibacteriële eigenschappen van cellen te versterken
Een nieuwe manier vinden om sepsis in een laat stadium te bestrijden door de antibacteriële eigenschappen van cellen te versterken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

