
Wetenschap
Welk element zal een edelgasconfiguratie hebben als het een ionische binding vormt door één elektron uit natriumatoom te accepteren?
Het element dat een edelgasconfiguratie zal hebben na het accepteren van één elektron uit een natriumatoom is chloor (CL) .
Dit is waarom:
* natrium (na) Heeft één valentie -elektron. Wanneer het dit elektron verliest, vormt het een +1 kation (Na +) en bereikt het de elektronenconfiguratie van neon (NE), een edelgas.
* chloor (Cl) heeft zeven valentie -elektronen. Wanneer het één elektron wint, vormt het een -1 anion (Cl-) en bereikt het de elektronenconfiguratie van argon (AR), een edelgas.
Daarom, wanneer natrium en chloor reageren, verliest natrium een elektron tot chloor, wat resulteert in de vorming van natriumchloride (NaCl). Beide ionen bereiken een stabiele edelgasconfiguratie, waardoor de ionische binding erg sterk is.
 Wat gebeurt er als u spuitverf en water mengt?
Wat gebeurt er als u spuitverf en water mengt?  Geometrisch verbijsterende quasikristallen gevonden in het puin van de allereerste nucleaire explosie
Geometrisch verbijsterende quasikristallen gevonden in het puin van de allereerste nucleaire explosie Wat deed Ernest Rutherford voor Atomic Theory?
Wat deed Ernest Rutherford voor Atomic Theory?  Scholes vindt nieuw magnetisch veldeffect in diamagnetische moleculen
Scholes vindt nieuw magnetisch veldeffect in diamagnetische moleculen Welk materiaal is niet ontvlambaar?
Welk materiaal is niet ontvlambaar?
 Wat is het deel aarde dat het leven ondersteunt?
Wat is het deel aarde dat het leven ondersteunt?  De ontdekking van Christmas Island hertekent de kaart van het leven
De ontdekking van Christmas Island hertekent de kaart van het leven Klimaatverandering overleven betekent een transformatie van zowel economie als design
Klimaatverandering overleven betekent een transformatie van zowel economie als design Waarom het afgelegen Antarctica zo belangrijk is in een opwarmende wereld
Waarom het afgelegen Antarctica zo belangrijk is in een opwarmende wereld Twee enorme stormen in twee weken, maar zijn het volledig natuurrampen?
Twee enorme stormen in twee weken, maar zijn het volledig natuurrampen?
Hoofdlijnen
- Coevolution: definitie, soorten en voorbeelden
- Model suggereert hoe de code van het leven uit de oersoep voortkwam
- Wat zijn de verschillen tussen de evolutietheorie en tegenstrijdige theorieën?
- Welk product van fotosyntgesis wordt gebruikt bij cellulaire ademhaling?
- Deze boom is het oudste levende organisme van Europa - een soort van,
- Wat is er nodig om de regent-honingeter te redden?
- Wat is Biological Forum?
- Wat zijn de verschillen tussen homozygote dominante en recessieve heterozygoot?
- Zal er ooit een gelukkige pil zijn?
- Onderzoekers krijgen inzicht in hoe enzymen specifieke reacties bereiken
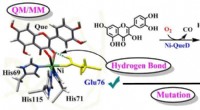
- Plantaardige alkaloïden beschermen rijst, kiwi en citrus van schadelijke bacteriën

- Hooggevoelige nanofotonische sensoren met passieve opsluiting van analytmoleculen in hotspots

- Noem die whisky:colorimetrische herkenning van aldehyden en ketonen
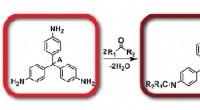
- Team ontwikkelt 's werelds eerste on-the-spot test voor synthetische drugskruiden

 Wat is de snelheid van een trein die 120 km per uur in de tweede uur reist?
Wat is de snelheid van een trein die 120 km per uur in de tweede uur reist?  Hoe de treksterkte van een U-bout te berekenen
Hoe de treksterkte van een U-bout te berekenen  Hoe dieren aan hun strepen en vlekken komen
Hoe dieren aan hun strepen en vlekken komen  Hoeveel gram is gelijk aan 27,5 mg?
Hoeveel gram is gelijk aan 27,5 mg?  Kan een verenigd pad voor ontwikkeling en behoud tot een betere toekomst leiden?
Kan een verenigd pad voor ontwikkeling en behoud tot een betere toekomst leiden?  Wat is het cluster van sterrenstelsels die zijn samengesteld door vijfentwintig inclusief Melkweg?
Wat is het cluster van sterrenstelsels die zijn samengesteld door vijfentwintig inclusief Melkweg?  Nieuwe methode maakt metingen van magnetisme met hoge resolutie mogelijk
Nieuwe methode maakt metingen van magnetisme met hoge resolutie mogelijk Kan temperatuur de geleidbaarheid van materiaal beïnvloeden?
Kan temperatuur de geleidbaarheid van materiaal beïnvloeden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

