
Wetenschap
Welk element in combinatie met fluor zou waarschijnlijk van een ionische verbinding?
Elementen in groep 1 (alkali metalen) en groep 2 (alkalische aardmetalen) zijn hiervoor de beste kandidaten.
Dit is waarom:
* Groep 1: Deze metalen hebben slechts één valentie -elektron, waardoor het relatief eenvoudig voor hen is om dat elektron te verliezen en een +1 kation te vormen.
* Groep 2: Deze metalen hebben twee valentie -elektronen, dus ze verliezen beide en vormen een +2 kation.
Voorbeelden:
* natrium (na) uit groep 1 zou natriumfluoride (NAF) vormen.
* calcium (ca) Uit groep 2 zou calciumfluoride (CAF₂) vormen.
Samenvattend: Elementen in groep 1 en groep 2, vanwege hun neiging om elektronen te verliezen, zouden waarschijnlijk ionische verbindingen met fluor vormen.
 Unboil een eiermachine zorgt voor een verbeterde bacteriedetector
Unboil een eiermachine zorgt voor een verbeterde bacteriedetector Als u in een experiment koper (II) sulfaat moest gebruiken en alleen met klonten sulfaat werd geleverd, welk hulpmiddel zou de bruikbare vorm nodig hebben?
Als u in een experiment koper (II) sulfaat moest gebruiken en alleen met klonten sulfaat werd geleverd, welk hulpmiddel zou de bruikbare vorm nodig hebben?  Zoete lysine-afbraak
Zoete lysine-afbraak Is het waar dat zwavel geen eenvoudig ion kan vormen?
Is het waar dat zwavel geen eenvoudig ion kan vormen?  Katalyseren enzymen in het spijsverteringskanaal hydrolysereacties?
Katalyseren enzymen in het spijsverteringskanaal hydrolysereacties?
 Japanse retailers brengen vanaf 2020 kosten in rekening voor plastic tassen
Japanse retailers brengen vanaf 2020 kosten in rekening voor plastic tassen Welke digitale revolutie? Honderden miljoenen boeren kunnen nog steeds niet online
Welke digitale revolutie? Honderden miljoenen boeren kunnen nog steeds niet online De effecten van overbevolking bij dieren
De effecten van overbevolking bij dieren  Opinie:Tijd om de uitdaging van klimaatverandering te heroverwegen
Opinie:Tijd om de uitdaging van klimaatverandering te heroverwegen Slechts 10 riviersystemen dragen tot 95 procent bij aan plastic in oceanen
Slechts 10 riviersystemen dragen tot 95 procent bij aan plastic in oceanen
Hoofdlijnen
- Wat zijn twee basis manieren waarop cellen een stof kunnen verteren?
- Waarom hitte gebruiken om de microbiële groei onder controle te houden?
- Wetenschappers werken aan een omkeerbare vorm van genbewerking
- Welke organel omringt elke cel?
- De vijand binnenin:hoe ziekteverwekkers zich ongemerkt in het lichaam verspreiden
- Wat wordt bedoeld met de zin DNA erfelijk materiaal?
- Koolhydraten worden gedefinieerd als wat?
- Welke eukaryoten die geen lid zijn van de Kingdoms Plantae Animalia of Fungi overwogen?
- Vogelgriep heeft melkveehouderijen in Idaho besmet:is de staat voorbereid op een uitbraak?
- Hoogwaardige katalysatoren met één atoom voor brandstofcellen bij hoge temperaturen

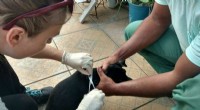
- Elektronische neus om honden te snuffelen voor dodelijke tropische ziekte in Brazilië
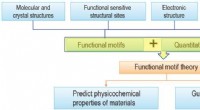
- De cruciale rol van functionele motieven—microstructurele eenheden die materiële functies bepalen—in materiaalonderzoek
- Een nieuwe benadering om de katalysatoren voor de waterstofevolutiereactie te verbeteren

- Iridium en 2-methylfenantroline versnellen katalytische boryleringsreacties

 Een sponsachtige moleculaire kooi voor zuivering van fullerenen
Een sponsachtige moleculaire kooi voor zuivering van fullerenen Twee vorderingen in het begrijpen van de rol van ladingsstrepen in supergeleidende mate
Twee vorderingen in het begrijpen van de rol van ladingsstrepen in supergeleidende mate Wat werken elektrische krachten tussen?
Wat werken elektrische krachten tussen?  Snelle tool ontwikkeld voor quantum computing en communicatie
Snelle tool ontwikkeld voor quantum computing en communicatie Alles wat de aarde wil voor Kerstmis? Een sok is steenkool
Alles wat de aarde wil voor Kerstmis? Een sok is steenkool  Skiërs gewond door rondvliegende stenen op Japanse vulkaan
Skiërs gewond door rondvliegende stenen op Japanse vulkaan Klimaataanwijzingen ijstijd opgegraven
Klimaataanwijzingen ijstijd opgegraven Nieuwe theorie zet wat we weten over hoe geladen macromoleculen zichzelf assembleren op zijn kop
Nieuwe theorie zet wat we weten over hoe geladen macromoleculen zichzelf assembleren op zijn kop
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

