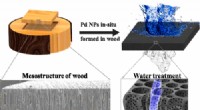
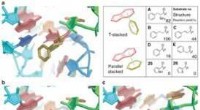
Wetenschap
Wat is de reactie tussen natriumhydride en waterstofsulfide?
Hier is de evenwichtige chemische vergelijking:
2 NAH + H₂s → Na₂s + 2 H₂
Verklaring:
* Natriumhydride (NAH) is een sterke basis en waterstofsulfide (H₂S) is een zwak zuur.
* De reactie verloopt door de overdracht van een proton (H⁺) van waterstofsulfide naar het hydride -ion (H⁻) van natriumhydride.
* Het resulterende natriumsulfide (NA₂S) is een zout, terwijl waterstofgas (H₂) wordt vrijgegeven als een bijproduct.
Belangrijke opmerking:
* Deze reactie is zeer exotherme, wat betekent dat het een aanzienlijke hoeveelheid warmte vrijgeeft.
* Het is essentieel om deze reactie uit te voeren met voorzichtigheid in een goed geventileerd gebied en onder de juiste veiligheidsmaatregelen vanwege de brandbare aard van waterstofgas.
 Chemici verkregen nieuwe verbinding voor moleculaire machines
Chemici verkregen nieuwe verbinding voor moleculaire machines In een oplossing is de hoeveelheid oplosmiddel?
In een oplossing is de hoeveelheid oplosmiddel?  Wat is de methode om mengselnitre en gewone zout te scheiden?
Wat is de methode om mengselnitre en gewone zout te scheiden?  ALLEEN DE PROTONEN DIE AAN KOOLSTOF GEBONDEN ZIJN, in volgorde van zuurgraad aflopend, de volgende verbindingen CH3CH2OH, CH3COCH3, CH3COH, CH3COOCH3?
ALLEEN DE PROTONEN DIE AAN KOOLSTOF GEBONDEN ZIJN, in volgorde van zuurgraad aflopend, de volgende verbindingen CH3CH2OH, CH3COCH3, CH3COH, CH3COOCH3?  Listeria-reproductie stoppen in zijn sporen
Listeria-reproductie stoppen in zijn sporen
Hoofdlijnen
- Wat zijn de beste nucleotide -drieling die een codon vertegenwoordigen?
- Wat is de meest gebruikelijke manier om bacteriën te laten groeien?
- Hoe dieren en planten eiwitten krijgen?
- Welk probleem zouden mensen hebben als ze geen fenylalaninehydroxylase gebruiken?
- Hoe een opkomende ziekte bij honden licht werpt op cystische fibrose
- Welke technologie werd mogelijk gemaakt door de ontdekking van structuur -DNA?
- Hoe schimmels hebben bijgedragen aan het creëren van leven zoals wij dat kennen
- Hoe worden lichaamscellen uitgescheiden?
- De temperatuur in cellen meten
 Laura voorspelt nu een catastrofale orkaan van categorie 4
Laura voorspelt nu een catastrofale orkaan van categorie 4 Wat zijn de fasen van water van het langzaamste tot snelste moleculair?
Wat zijn de fasen van water van het langzaamste tot snelste moleculair?  Broomwater maken in de chemie Lab
Broomwater maken in de chemie Lab Hoe functioneert glycogeen in levende dingen?
Hoe functioneert glycogeen in levende dingen?  Wat eet tentrupsbanden?
Wat eet tentrupsbanden?  Welke soorten energie verspilt een gasketel?
Welke soorten energie verspilt een gasketel?  De geest heeft de geest van de maan overgenomen:hoe Torres Strait Islanders verduisteringen voorspellen
De geest heeft de geest van de maan overgenomen:hoe Torres Strait Islanders verduisteringen voorspellen  Hubble is de ultieme multitasker:asteroïden ontdekken terwijl hij andere waarnemingen doet
Hubble is de ultieme multitasker:asteroïden ontdekken terwijl hij andere waarnemingen doet
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com