
Wetenschap
Hoeveel moleculen van H20 zijn er in 2,43 mol H20?
Inzicht in het concept
* mol (mol): Een mol is een meeteenheid die een specifiek aantal deeltjes vertegenwoordigt (atomen, moleculen, ionen, enz.). Eén mol is gelijk aan deeltjes van 6,022 x 10²³, wat bekend staat als het nummer van Avogadro.
Berekening
1. Avogadro's nummer: We zullen het nummer van Avogadro (6.022 x 10²³) gebruiken als de conversiefactor tussen mol en moleculen.
2. Stel de conversie in:
* (2.43 mol H₂o) x (6.022 x 10²³ Moleculen H₂o / 1 mol H₂o)
3. Annuleer de eenheden: Merk op hoe de "mol h₂o" -eenheden annuleren, waardoor we "moleculen h₂o" achterlaten.
4. Bereken:
* 2.43 x 6.022 x 10²³ =1,46 x 10²⁴ Moleculen H₂o
Antwoord: Er zijn ongeveer 1,46 x 10²⁴ moleculen van H₂o In 2.43 mol H₂o.
 Welke anorganische ionen worden vrijgegeven door de dissociatie van elektrolyten?
Welke anorganische ionen worden vrijgegeven door de dissociatie van elektrolyten?  Nieuwe tijdsopgeloste ultraviolette fotodissociatie-massaspectrometriestrategie voor analyse van de stabiliteit van doeleiwitten
Nieuwe tijdsopgeloste ultraviolette fotodissociatie-massaspectrometriestrategie voor analyse van de stabiliteit van doeleiwitten  Wetenschappers duwen microscopie naar submoleculaire resolutie
Wetenschappers duwen microscopie naar submoleculaire resolutie Vaste stoffen vloeistoffen en gassen. Welke zijn moeilijk te vervormen?
Vaste stoffen vloeistoffen en gassen. Welke zijn moeilijk te vervormen?  Is smaakverandering een chemische reactie?
Is smaakverandering een chemische reactie?
Hoofdlijnen
- Een celorganel die voedselmoleculen afbreekt en energie vrijgeeft?
- Welk type mensen leven in het chaparral-bioom?
- Sint-jakobsschelpen hebben 200 ogen, die functioneren als een telescoop:studie
- Waarom gebruiken wetenschappers massa in plaats van gewicht?
- Wat is de mobiele organisatie van Archaea?
- Wat is conclusie in de wetenschappelijke methode?
- Nieuw algoritme herkent duidelijke dolfijnklikken in onderwateropnamen
- Onderzoek werpt licht op hoe bladsnijdermieren chemische afscheidingen gebruiken om schimmelinfecties te voorkomen
- Genoomsequencing onthult uitgebreide inteelt bij Scandinavische wolven
- Biologisch afbreekbare kunststoffen uit palmolieafval

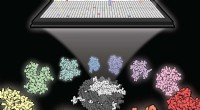
- Duizenden moleculen scannen tegen een ongrijpbaar kankerdoelwit
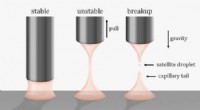
- Een nieuwe draai om visco-elastische vloeistofbruggen te doorbreken
- Miljoenen blootgesteld aan potentieel gevaarlijke metalen, nieuwe technologie kan het risico helpen verlagen
- Video:Petrichor, de geur van regen

 Hoeveel bindingen kan de ene koolstofatoom vormen met een ander atoom?
Hoeveel bindingen kan de ene koolstofatoom vormen met een ander atoom?  Omdat prokaryoten niet veel specifieke structuren hebben, wat dan?
Omdat prokaryoten niet veel specifieke structuren hebben, wat dan?  Wat is tamme gist?
Wat is tamme gist?  Pandemische vuilnisbelt ontketent debat over afval als energie
Pandemische vuilnisbelt ontketent debat over afval als energie Thermische ontleding en temperatuur:verwijzen dit naar dezelfde dingen?
Thermische ontleding en temperatuur:verwijzen dit naar dezelfde dingen?  Chinees bedrijf kondigt ontwikkeling van elektronisch grafeenpapier aan
Chinees bedrijf kondigt ontwikkeling van elektronisch grafeenpapier aan Wanneer energie in een transformatie verloren is gegaan, waar gaat het dan heen?
Wanneer energie in een transformatie verloren is gegaan, waar gaat het dan heen?  Wat bevat de troposfeer?
Wat bevat de troposfeer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

