
Wetenschap
Waarom worden de hoeveelheden producten gevormd in een reactie die alleen wordt bepaald door de reactant te beperken?
1. Beperkende reactant:
* De beperkende reactant is de reactant die volledig wordt geconsumeerd in een chemische reactie.
* Het stelt een bovengrens vast voor hoeveel product kan worden gevormd.
2. Overtollige reactant:
* De overtollige reactant is de reactant die niet volledig wordt geconsumeerd in een chemische reactie.
* Het heeft nog wat bedrag over nadat de reactie is voltooid.
3. De stoichiometrie van de reactie:
* De evenwichtige chemische vergelijking voor de reactie biedt de stoichiometrische verhoudingen van reactanten en producten. Dit betekent dat het ons de precieze hoeveelheden vertelt van elke stof die bij de reactie betrokken is.
Hier is hoe het werkt:
1. Stel je een recept voor: Je hebt een recept voor koekjes dat 2 kopjes bloem en 1 kopje suiker vereist. Als je maar 1 kopje bloem hebt, kun je slechts de helft van de hoeveelheid koekjes maken, zelfs als je veel suiker hebt. De bloem is de beperkende reactant.
2. De beperkende reactant is eerst opgelopen: In een chemische reactie wordt de beperkende reactant volledig opgebruikt vóór de andere reactanten. Zodra het weg is, stopt de reactie.
3. Er kan geen product meer worden gevormd: Omdat de reactie stopt wanneer de beperkende reactant wordt opgebruikt, kan er geen product meer worden gevormd, zelfs als er meer dan andere reactanten zijn.
Voorbeeld:
Laten we zeggen dat u 10 gram natrium (NA) en 10 gram chloor (CL) heeft die reageert op natriumchloride (NaCl):
`` `
2 Na + Cl2 → 2 NaCl
`` `
* Stap 1:Bereken Moles: Bereken de mol van elke reactant met behulp van hun molaire massa's.
* Stap 2:Bepaal de beperkende reactant: Vergelijk de molverhoudingen van de reactanten op basis van de stoichiometrie van de reactie. De reactant met de lagere molverhouding (ten opzichte van de coëfficiënten in de gebalanceerde vergelijking) is de beperkende reactant.
* Stap 3:Bereken de hoeveelheid product: De hoeveelheid gevormde product wordt bepaald door het bedrag van de beperkende reactant die wordt verbruikt.
Samenvattend: De beperkende reactant regelt de hoeveelheid gevormde product omdat het de eerste is die volledig wordt geconsumeerd, waardoor de reactie wordt gestopt en verdere productvorming wordt voorkomen.
 Degraderende permafrost brengt de Arctische infrastructuur tegen het midden van de eeuw in gevaar
Degraderende permafrost brengt de Arctische infrastructuur tegen het midden van de eeuw in gevaar Rustig voor storm? Vreemd rustige Atlantische Oceaan ondanks voorspellingen
Rustig voor storm? Vreemd rustige Atlantische Oceaan ondanks voorspellingen Klimaatverandering verhoogt de vastlegging van blauwe koolstof aan de kust
Klimaatverandering verhoogt de vastlegging van blauwe koolstof aan de kust Door de moessonoverstromingen zijn duizenden gestrand in India
Door de moessonoverstromingen zijn duizenden gestrand in India Naar huis vliegen? De ijstijd heeft mogelijk de vogelmigratie afgeremd
Naar huis vliegen? De ijstijd heeft mogelijk de vogelmigratie afgeremd
Hoofdlijnen
- Van het verpletteren van zee-egels tot in het laboratorium gekweekte kelp:de inspanningen om de kelpbossen in Californië te redden zijn veelbelovend
- Hoe worden protisten geclassificeerd?
- Waarom zijn de buitenste bedekkingen belangrijk voor beweging in veel ongewervelde dieren?
- Microben die gaatjes veroorzaken, kunnen superorganismen vormen die kunnen kruipen en zich op de tanden kunnen verspreiden
- Wat is het kleine lichaam in de kern die ribosomen verzamelt?
- Wat produceert in de hersenen secreties die de lichaamsfunctie regelen?
- Hebben alle cellen dezelfde samenstelling?
- Wat is de route die door mucine door cel is genomen door de synthese van de secretie om alle betrokken organellen en processen te vermelden?
- Bloemstroken en heggen geven samen een boost aan bijen in boomgaarden
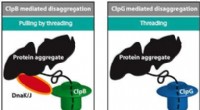
- Hoe ontvouwen cellulaire machines verkeerd gevouwen eiwitten?
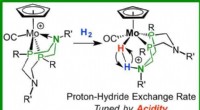
- Wetenschappers bepalen de snelheid van het breken en fixeren van diwaterstofmoleculen
- Bioluminescente succinaatdetectie bewaakt dioxygenasen en JMJC-demethylasen

- Magnetische T-Budbots gemaakt van theeplanten doden en reinigen biofilms

- Onderzoek wat titanium implantaten hun opmerkelijke biocompatibiliteit geeft

 Bevinden de sterren zich ten opzichte van de hemelse bol op het oppervlak van de bol?
Bevinden de sterren zich ten opzichte van de hemelse bol op het oppervlak van de bol?  Wat is het verschil in wit gat en zwart in astronomie?
Wat is het verschil in wit gat en zwart in astronomie?  Wat is de voedselketen voor het Woodlands-ecosysteem?
Wat is de voedselketen voor het Woodlands-ecosysteem?
Voedselketens beschrijven 'wat eet wat' in een ecosysteem. Er bestaat geen voedselketen voor een bosecosysteem, omdat er vele soorten bosecosystemen bestaan en, binnen die systemen, veel elkaa
 Welke ster is het koudste ster?
Welke ster is het koudste ster?  Welk instrument produceert patronen die een aardbeving aangeven?
Welk instrument produceert patronen die een aardbeving aangeven?  NASA volgt orkaan Olivias richting Hawaï
NASA volgt orkaan Olivias richting Hawaï Wat zijn de specificaties en kwaliteiten voor stikstofzuiverheid?
Wat zijn de specificaties en kwaliteiten voor stikstofzuiverheid?  Een vaas zit op een plank welke vorm van energie bezit het?
Een vaas zit op een plank welke vorm van energie bezit het?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

