
Wetenschap
Hoeveel mol ammomiumhydroxide zijn aanwezig in 0,475 g?
Hier leest u hoe u de mol ammoniumhydroxide (NH₄OH) aanwezig kunt berekenen in 0,475 g:
1. Vind de molaire massa van NH₄OH:
* N:14.01 g/mol
* H:1,01 g/mol (er zijn 5 waterstofatomen)
* O:16.00 g/mol
Totale molaire massa =14,01 + (1,01 x 5) + 16.00 =35,06 g/mol
2. Gebruik de formule:moles =massa / molaire massa
* mol =0,475 g / 35,06 g / mol
* mol ≈ 0,0136 mol
Daarom zijn ongeveer 0,0136 mol ammoniumhydroxide aanwezig in 0,475 g
 Atmosferische salpeterigzuurchemie onthult een aanzienlijk onderschatte oxidatiecapaciteit in Noord-China
Atmosferische salpeterigzuurchemie onthult een aanzienlijk onderschatte oxidatiecapaciteit in Noord-China MABI-instrument kan de concentratie en bron van zwarte koolstofvervuiling in de atmosfeer bepalen
MABI-instrument kan de concentratie en bron van zwarte koolstofvervuiling in de atmosfeer bepalen Brits cruiseschip beschadigt ongerept Indonesisch koraalrif
Brits cruiseschip beschadigt ongerept Indonesisch koraalrif Trump klaar om regels voor kolencentrales te versoepelen
Trump klaar om regels voor kolencentrales te versoepelen Cycloon Mekunu intensiveert naarmate hij verder komt op Oman
Cycloon Mekunu intensiveert naarmate hij verder komt op Oman
Hoofdlijnen
- Zijn menselijke klonen gehaat door mensen?
- Doorbraak helpt verklaren hoe DNA in onze cellen is georganiseerd
- Hoe extremofielen werken
- Aquatische wiet behoort tot de ergste ter wereld en breidt zich uit in het noordoosten van de VS
- Wat helpt om eiwitten in een cel te maken?
- Was de eerste wetenschapper die onderzoek doet hoe ziekte levende wezens beïnvloedt?
- Kill-schakelaars voor gemanipuleerde microben die schurkenstaten zijn geworden
- Kunnen bevers een chronische slopende ziekte krijgen?
- Een geërfd kenmerk dat het vermogen van een organismen vergroot om te overleven en zich in zijn specifieke omgeving te reproduceren, wordt een genoemd?
- Door meniscus ondersteunde techniek produceert perovskiet PV-films met een hoog rendement

- Volatiliteitsverrassingen ontstaan bij het verwijderen van overtollig waterstof

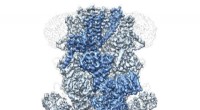
- Cryo-EM onthult structuur van eiwit dat verantwoordelijk is voor het reguleren van de lichaamstemperatuur
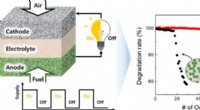
- Lager nikkelgehalte en verbeterde stabiliteit en prestaties in keramische brandstofcellen
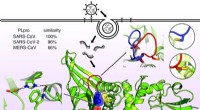
- Informatie over de moleculaire vorm van virussen die COVID-19 veroorzaken, SARS, en MERS onthult structurele overeenkomsten
 Atomen in alle verbindingen worden bij elkaar gehouden door krachten die?
Atomen in alle verbindingen worden bij elkaar gehouden door krachten die?  Harley-Davidson schort productie elektrische motorfiets op
Harley-Davidson schort productie elektrische motorfiets op De pandemie heeft de kloof tussen arm en rijk vergroot, en het gaat door
De pandemie heeft de kloof tussen arm en rijk vergroot, en het gaat door Hoe past bij de voornaamste bewegingsmachine de principe van natuurbeschermingsenergie?
Hoe past bij de voornaamste bewegingsmachine de principe van natuurbeschermingsenergie?  Waarom schieten schietsterren aan de nachtelijke hemel?
Waarom schieten schietsterren aan de nachtelijke hemel?  Is afstand een grootte van de gemiddelde snelheid?
Is afstand een grootte van de gemiddelde snelheid?  Waarom kan een betere resolutie worden bereikt met een optische microscoop die blauw licht gebruikt in plaats van rood licht?
Waarom kan een betere resolutie worden bereikt met een optische microscoop die blauw licht gebruikt in plaats van rood licht?  Onderzoekers meten hoe lief de deal is voor zakelijke politieke donoren
Onderzoekers meten hoe lief de deal is voor zakelijke politieke donoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

