
Wetenschap
Wat is de evenwichtige vergelijking voor bariumnitraat en kaliumfosfaat?
1. Schrijf de onevenwichtige vergelijking:
Ba (no₃) ₂ (aq) + k₃po₄ (aq) → ba₃ (po₄) ₂ (s) + kno₃ (aq)
2. Breng de vergelijking in evenwicht:
* Barium (BA): Er zijn 3 BA -atomen aan de productzijde en 1 aan de reactantzijde. Voeg een coëfficiënt van 3 toe voor BA (No₃) ₂.
* fosfaat (PO₄): Er zijn 2 PO₄ -groepen aan de productzijde en 1 aan de reactantzijde. Voeg een coëfficiënt van 2 toe voor k₃po₄.
* kalium (k): Nu zijn er 6 K -atomen aan de reactantzijde (2 x 3) en we hebben 6 aan de productzijde nodig. Voeg een coëfficiënt van 6 toe voor kno₃.
* nitraat (no₃): Er zijn 6 no₃ -groepen aan de productzijde en 6 aan de reactantzijde (3 x 2).
3. Evenwichtige vergelijking:
3BA (no₃) ₂ (aq) + 2k₃po₄ (aq) → ba₃ (po₄) ₂ (s) + 6Kno₃ (aq)
Verklaring:
* Deze reactie is een dubbele verplaatsingsreactie , waar de kationen en anionen van de reactanten van plaats schakelen.
* Het productbariumfosfaat (ba₃ (po₄) ₂) is onoplosbaar in water, dus het vormt een neerslag (s).
* Het andere product, kaliumnitraat (kno₃), blijft opgelost in water (aq).
 Hoe 'Dune' een baken werd voor de jonge milieubeweging en een strijdkreet voor de nieuwe wetenschap van de ecologie
Hoe 'Dune' een baken werd voor de jonge milieubeweging en een strijdkreet voor de nieuwe wetenschap van de ecologie  Aanwijzingen uit diepe magmareservoirs kunnen de voorspellingen van vulkaanuitbarstingen verbeteren
Aanwijzingen uit diepe magmareservoirs kunnen de voorspellingen van vulkaanuitbarstingen verbeteren  Kenmerken van zaadloze vaatplanten
Kenmerken van zaadloze vaatplanten  Hoe wordt de stikstofcyclus door het ecosysteem?
Hoe wordt de stikstofcyclus door het ecosysteem?  Hoe helpt het Antropoceen de hedendaagse kwestie van de achteruitgang van het milieu te heroverwegen?
Hoe helpt het Antropoceen de hedendaagse kwestie van de achteruitgang van het milieu te heroverwegen?
Hoofdlijnen
- Wat worden hulpmiddelen gebruikt om de biosfeer te bestuderen?
- Een gen wiens code niet wordt uitgedrukt tenzij er een soortgelijk allel aanwezig wordt genoemd?
- Welk deel van de gastheer eten bacteriën en virussen?
- Wat is de structuur van Phloem?
- Hoe kan zuurstof naar de cellen worden uitgehongerd?
- Natuurlijke selectie werkt op variatie door?
- Welk organisme wordt gebruikt om gisting te bestuderen?
- Wat zijn de dingen die wetenschap niet kan beantwoorden of doen?
- Wat maakt plantencelwanden zowel sterk als uitbreidbaar?
- Video:Hoe rubber sporten mogelijk maakt

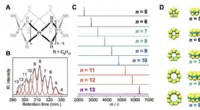
- Een reactie op preparatieve schaal met behulp van platinaclusters met een gerealiseerde eencijferige atomiciteit
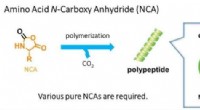
- Het beste van twee werelden:basis-naar-zure flitsschakeling voor organische synthese
- Zetmeel kan normaal plastic in voedselverpakkingen vervangen

- Het toevoegen van een inert polymeer aan plastic zonnecellen zorgt voor een hoog rendement en eenvoudige productie

 Gepofte rijst gebruiken om instortende ijsplaten en stortdammen te simuleren
Gepofte rijst gebruiken om instortende ijsplaten en stortdammen te simuleren Hoe complottheoretici de COVID-19-wetenschap uitbuitten
Hoe complottheoretici de COVID-19-wetenschap uitbuitten Wat is de valentie van bromide?
Wat is de valentie van bromide?  Welk biochemisch proces is verantwoordelijk voor koolstoffixatie?
Welk biochemisch proces is verantwoordelijk voor koolstoffixatie?  Vloeistoffen die geen vorm in lagen mengen wanneer ze dichtheden hebben?
Vloeistoffen die geen vorm in lagen mengen wanneer ze dichtheden hebben?  Moleculaire hopper klein genoeg om enkele DNA-strengen te verplaatsen
Moleculaire hopper klein genoeg om enkele DNA-strengen te verplaatsen Wat zijn subsets of Real Numbers?
Wat zijn subsets of Real Numbers?  Wat is een arctische vlakte met sub-layer van permafrost?
Wat is een arctische vlakte met sub-layer van permafrost?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

