
Wetenschap
Zou u verwachten dat natriumfluoride dezelfde kleur produceert als chloride en waarom?
* vlamtests en elektronenexcitatie: Vlamtests werken door een monster in een vlam te introduceren. De warmte van de vlam boeit elektronen in de metaalatomen. Wanneer deze opgewonden elektronen terugkeren naar hun grondtoestand, stoten ze het licht uit van een specifieke golflengte en produceren ze de karakteristieke kleur.
* Verschillende elektronenconfiguraties: Natriumfluoride (NAF) en natriumchloride (NaCl) hebben verschillende anioncomponenten (fluoride en chloride). Fluor en chloor hebben verschillende aantallen elektronen en verschillende elektronische configuraties. Dit betekent dat hun elektronen enthousiast zullen zijn voor verschillende energieniveaus in de vlam, wat resulteert in de emissie van verschillende golflengten van licht.
* waargenomen kleuren: Natriumchloride produceert een felgeel-oranje kleur in een vlamtest vanwege de excitatie van het buitenste elektron van natrium. Natriumfluoride produceert daarentegen een lichtgele kleur, die minder intens is en dichter bij wit lijkt, afhankelijk van de vlamomstandigheden.
Samenvattend: Hoewel beide verbindingen natrium bevatten, leiden de verschillen in hun anionische componenten tot verschillende kleuremissies in vlamtests.
 Onderzoekers ontwikkelen genetisch hulpmiddel om arseenstudies te verbeteren
Onderzoekers ontwikkelen genetisch hulpmiddel om arseenstudies te verbeteren Californië en het Westen braden in recordhittegolf
Californië en het Westen braden in recordhittegolf Vergroening op hoge breedtegraden kan de uitbreiding van woestijnen op gemiddelde breedtegraden remmen
Vergroening op hoge breedtegraden kan de uitbreiding van woestijnen op gemiddelde breedtegraden remmen Hoe spreken wetenschap en bijgelovig elkaar tegen?
Hoe spreken wetenschap en bijgelovig elkaar tegen?  Wat wordt spiritueel bedoeld met fotosynthese?
Wat wordt spiritueel bedoeld met fotosynthese?
Hoofdlijnen
- Wat is de oorsprong van Sinterklaas?
- Gespecialiseerde eilandjescellen die hormonen afscheiden worden verspreid over de?
- Wanneer komt organogenese op?
- Wetenschappers laten zien hoe enkele van de vroegste dieren op aarde evolueerden
- Onderzoek wijst uit dat de meest nuttige habitat is voor de minste vliegenvanger
- Radiometrische datering: definitie, hoe werkt het, gebruik & voorbeelden
- Wat is een betekenishypothese?
- Welk deel van de hibiscus wordt gebruikt?
- Betekent Alphabet succes voor Google?
- Zelfvoorzienende lus van chemische reacties kan een revolutie teweegbrengen in de productie van geneesmiddelen
- Nieuwe familie van selectieve op zilver gebaseerde geneesmiddelen tegen kanker ontdekt
- Een eenvoudige methode ontwikkeld voor 3D-biofabricage op basis van bacteriële cellulose

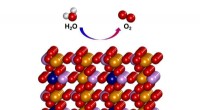
- Elektrokatalysator vertoont uitstekende watersplitsingsactiviteit
- Oorzaken van aantasting van beton en asfalt uitgelegd

 Chinas Trip.com zegt dat topmanagers niet worden betaald terwijl het virus woedt
Chinas Trip.com zegt dat topmanagers niet worden betaald terwijl het virus woedt Zeewaterbacteriën bieden aanknopingspunten om melanoom te bestrijden
Zeewaterbacteriën bieden aanknopingspunten om melanoom te bestrijden Welke twee factoren bepalen de snelheid van een object?
Welke twee factoren bepalen de snelheid van een object?  Waarom is de lucht op een heldere dag witter naar Horizon?
Waarom is de lucht op een heldere dag witter naar Horizon?  Miljoenen bomen meer is niet de klimaatoplossing die Nieuw-Zeeland dacht
Miljoenen bomen meer is niet de klimaatoplossing die Nieuw-Zeeland dacht  Hoe gebruiken planten de voedingsstoffen en water om voedsel of glucose te produceren?
Hoe gebruiken planten de voedingsstoffen en water om voedsel of glucose te produceren?  Op welke snelheid reizen elektromagnetische golven door de ruimte?
Op welke snelheid reizen elektromagnetische golven door de ruimte?  Een natuurlijk geïnspireerde, herbruikbaar systeem dat water zuivert en zichzelf opbouwt
Een natuurlijk geïnspireerde, herbruikbaar systeem dat water zuivert en zichzelf opbouwt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

