
Wetenschap
Welke is groter silicium of zwavel?
Dit is waarom:
* Trends voor atoommaat: Atomaire grootte neemt in het algemeen toe naarmate u een groep (kolom) op de periodiek systeem naar beneden verplaatst. Dit komt omdat u bij elke periode een extra elektronenschaal toevoegt.
* Locatie: Silicium (SI) bevindt zich in groep 14, terwijl zwavel (s) zich in groep 16 bevindt. Beide bevinden zich in de derde periode.
* elektronegativiteit: Zwavel is elektronegatiefer dan silicium, wat betekent dat het een sterkere trek heeft op zijn elektronen. Dit draagt ook bij aan zijn grotere atoomgrootte.
Daarom bevindt zwavel zich verderop in het periodiek systeem en heeft een grotere atoomgrootte dan silicium.
 Wat is het percentage samenstelling van gas op aarde?
Wat is het percentage samenstelling van gas op aarde?  Een stof in bruinkool kan virussen helpen bestrijden
Een stof in bruinkool kan virussen helpen bestrijden Kijken hoe een covalent polymeer zich ontwikkelt met behulp van een scanning tunneling microscoop
Kijken hoe een covalent polymeer zich ontwikkelt met behulp van een scanning tunneling microscoop Welke hybridisatie is aanwezig in een octaëdrische moleculaire geometrie?
Welke hybridisatie is aanwezig in een octaëdrische moleculaire geometrie?  Helium is essentieel voor onderzoek en medische apparatuur, maar het is niet hernieuwbaar en moeilijk te recyclen
Helium is essentieel voor onderzoek en medische apparatuur, maar het is niet hernieuwbaar en moeilijk te recyclen
 Blad op het eerste gezicht:hoe bladkrullende spinnen paren en een gezinswoning bouwen
Blad op het eerste gezicht:hoe bladkrullende spinnen paren en een gezinswoning bouwen  Wat is individueel VS -universum?
Wat is individueel VS -universum?  Buitenaardsen? laseren? Water? Wat zorgde ervoor dat de Al Naslaa-rots zo precies werd gespleten?
Buitenaardsen? laseren? Water? Wat zorgde ervoor dat de Al Naslaa-rots zo precies werd gespleten? Een zwak magnetisch veld heeft mogelijk de diversificatie van het leven op aarde ondersteund
Een zwak magnetisch veld heeft mogelijk de diversificatie van het leven op aarde ondersteund  Storm Katia bouwt op in het Caribisch gebied terwijl Irma toeslaat
Storm Katia bouwt op in het Caribisch gebied terwijl Irma toeslaat
Hoofdlijnen
- Hadeda ibissen zesde zintuig werkt het beste op natte grond:nieuw onderzoek is een wake-up call voor het voortbestaan van waadvogels
- Onderzoek onthult gebreken in populaire genetische methode
- Wetenschappers ontwikkelen een nieuwe geochemische vingerafdruk om verontreinigingen in kunstmest op te sporen
- Bacterieel model helpt onthullen hoe ons lichaam bevolkingsexplosies – en kanker – voorkomt
- Hoeveel wetenschapsvelden zijn er?
- Waar bevindt het metabolisme zich?
- Een zenuwcel die nooit in een volwassene verdeelt, is welke fase van de cyclus?
- Onderzoekers onderzoeken de impact van verhoogde CO₂-concentratie op subtropische bomen
- Wat kun je afleiden als de functie van het diafragma in een microscoop?
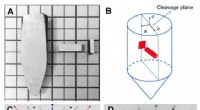
- Hoge thermo-elektrische prestaties in goedkope SnS0.91Se0.09-kristallen
- Op papier gebaseerde technologie bevordert eerdere kankerdetectie

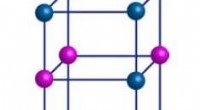
- Opvallen:ongebruikelijke magnetische overgang in perovskietoxide kan spintronica helpen stimuleren
- Knipper en je zult amyloïden niet missen

- Kokosolieverbindingen stoten insecten beter af dan DEET

 Waarom moet je energie produceren energie?
Waarom moet je energie produceren energie?  Kationmenging induceert zeer efficiënte natriumopslag voor gelaagde kathoden
Kationmenging induceert zeer efficiënte natriumopslag voor gelaagde kathoden Waar ging het einde van 2001 een ruimte -odyssee over?
Waar ging het einde van 2001 een ruimte -odyssee over?  Welke structuren worden gemaakt op de oceanische continentale convergentiegrens?
Welke structuren worden gemaakt op de oceanische continentale convergentiegrens?  Nieuwe sensor meet calciumconcentraties diep in weefsel
Nieuwe sensor meet calciumconcentraties diep in weefsel Microsoft neemt webdomeinen in beslag die worden gebruikt door Noord-Koreaanse hackers
Microsoft neemt webdomeinen in beslag die worden gebruikt door Noord-Koreaanse hackers Onderzoekers werken aan een beter begrip van hydrodynamische instabiliteiten in NIF, astrofysica
Onderzoekers werken aan een beter begrip van hydrodynamische instabiliteiten in NIF, astrofysica Nieuw inzicht in de oorsprong van water op aarde
Nieuw inzicht in de oorsprong van water op aarde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

