
Wetenschap
Wat gebeurt er in de reactie tussen salicylzuur en natriumhydroxide?
Hier is de evenwichtige chemische vergelijking:
c₇h₆o₃ (salicylzuur) + NaOH (natriumhydroxide) → C₇h₅o₃na (natriumsalicylaat) + H₂o (water)
Verklaring:
* salicylzuur (C₇h₆o₃) is een zwak organisch zuur met een carboxylgroep (-cooh) die een proton kan doneren (H⁺).
* Natriumhydroxide (NaOH) is een sterke basis die gemakkelijk hydroxide -ionen doneert (OH⁻).
Wanneer deze twee reageren, verwijdert het hydroxide -ion (OH⁻) van NaOH het zure proton (H⁺) uit de carboxylgroep van salicylzuur, waardoor water (H₂o) wordt gevormd. Het resterende natriumion (Na⁺) bindt met het salicylaation (c₇h₅o₃⁻) om natriumsalicylaat te vormen (C₇h₅o₃na).
Sleutelpunten:
* De reactie is exotherme, wat betekent dat het warmte vrijgeeft.
* Natriumsalicylaat is een zout en is meer oplosbaar in water dan salicylzuur. Deze reactie wordt vaak gebruikt om een oplossing van natriumsalicylaat te bereiden, die in verschillende toepassingen kan worden gebruikt, zoals farmaceutische producten en cosmetica.
* Deze reactie is een voorbeeld van een zuurbasisreactie waarbij een sterke basis een zwak zuur neutraliseert.
Laat het me weten als je nog vragen hebt!
 Wat is de kristalvorm van fluoriet?
Wat is de kristalvorm van fluoriet?  Wat scheidt de metalen en niet -metalen op periodieke tabel?
Wat scheidt de metalen en niet -metalen op periodieke tabel?  Wat is chemische formule voor stannic hypoiodiet?
Wat is chemische formule voor stannic hypoiodiet?  Enzymatische photocaging voor de studie van genregulatie door middel van DNA-methylatie
Enzymatische photocaging voor de studie van genregulatie door middel van DNA-methylatie Wat is de dichtheid van een monster zinkmetaal van 200 g of 500 g?
Wat is de dichtheid van een monster zinkmetaal van 200 g of 500 g?
 Kunnen we dinosaurussen doen herrijzen uit fossiele embryo's?
Kunnen we dinosaurussen doen herrijzen uit fossiele embryo's?  Wat is het resultaat van natuurlijke selectie?
Wat is het resultaat van natuurlijke selectie?  In een gevaarlijk opwarmende wereld moet de grimmige realiteit van de uitstoot van bosbranden in Australië onder ogen worden gezien
In een gevaarlijk opwarmende wereld moet de grimmige realiteit van de uitstoot van bosbranden in Australië onder ogen worden gezien  NASA volgt post-tropische cycloon Barry naar Indiana
NASA volgt post-tropische cycloon Barry naar Indiana Studie:Klimaatverandering treft kinderen onevenredig
Studie:Klimaatverandering treft kinderen onevenredig
Hoofdlijnen
- Welk type macromolecuul vormt de meeste membraanstructuur?
- Welke chemische bindingen hebben deze macromoleculen koolhydraat eiwit nucleïnezuur lipide?
- Welke methode zou u gebruiken om organismen te verdelen in groepenklassen op basis van specifieke kenmerken?
- Populaties van organismen evolueren voortdurend welke middelen?
- Beschrijf hoe ATP wordt gevormd?
- Wat voert een wetenschapper uit om gegevens te verzamelen nadat hij hypothese heeft gemaakt?
- Wat regelt de activiteit van melanocyten?
- 12-jarige studie van straatkatten onthult hoe populatieaantallen met succes onder controle kunnen worden
- Welk organel is verantwoordelijk voor de afvalverwerking en recycling in een dierlijke cel?
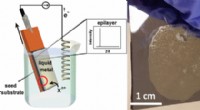
- Een goedkopere, groenere manier om kristallijne halfgeleiderfilms te kweken
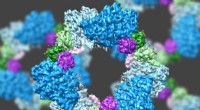
- Wetenschappers geven een glimp met hoge resolutie van de enzymstructuur
- Nieuw onderzoek toont de beperkingen van coördinatie in de chemie aan

- Nieuwe methode om zware omstandigheden voor materialen na te bootsen

- Experimentele natuurkundigen bestuderen staal aan boord van het ISS

 Vuurslimme landbouw:hoe de gewassen die we planten het risico op bosbranden in landbouwlandschappen kunnen helpen verminderen
Vuurslimme landbouw:hoe de gewassen die we planten het risico op bosbranden in landbouwlandschappen kunnen helpen verminderen  Waarom afneemt dat volume gas afneemt bij toenemende druk IT bij constante temperatuur?
Waarom afneemt dat volume gas afneemt bij toenemende druk IT bij constante temperatuur?  Hoe verschillen atomen van ionen?
Hoe verschillen atomen van ionen?  Waarom bewegen de bladeren van een geladen elektroscoop verder uit elkaar als de staaf met dezelfde lading dichtbij wordt gebracht?
Waarom bewegen de bladeren van een geladen elektroscoop verder uit elkaar als de staaf met dezelfde lading dichtbij wordt gebracht?  Welke samengestelde verbindingen aan zuurstof in rode bloedcellen?
Welke samengestelde verbindingen aan zuurstof in rode bloedcellen?  Hoe reageert de korst van onderaf op warmte?
Hoe reageert de korst van onderaf op warmte?  Enorme tweelingster ontdekt knuffelend dicht bij zijn stellaire broer of zus in zijn wieg
Enorme tweelingster ontdekt knuffelend dicht bij zijn stellaire broer of zus in zijn wieg Omgekeerd ontwerp van poreuze materialen met behulp van kunstmatige neurale netwerken
Omgekeerd ontwerp van poreuze materialen met behulp van kunstmatige neurale netwerken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

