
Wetenschap
Wat is de elektronische structuur van een chlooratoom 2 8 7?
* 2, 8, 7 vertegenwoordigt het aantal elektronen in elk van de elektronenschalen van het chlooratoom.
* shell 1: Bevat 2 elektronen (weergegeven door de '2').
* shell 2: Bevat 8 elektronen (weergegeven door de '8').
* shell 3: Bevat 7 elektronen (weergegeven door de '7').
Hier is een meer gedetailleerde uitsplitsing:
* 1S²: Dit betekent dat er 2 elektronen zijn in het eerste energieniveau (shell 1), dat ook de "S" subshell wordt genoemd.
* 2s² 2p⁶: Dit betekent dat er 8 elektronen zijn in het tweede energieniveau (shell 2), met 2 elektronen in de "S" subshell en 6 in de "P" subshell.
* 3S² 3P⁵: Dit betekent dat er 7 elektronen zijn in het derde energieniveau (Shell 3), met 2 elektronen in de "S" subshell en 5 in de "P" subshell.
Belangrijke opmerking: De elektronische configuratie helpt ons het chemische gedrag van chloor te begrijpen. Het heeft 7 elektronen in zijn buitenste schaal (valentie -elektronen), waardoor het zeer reactief is en waarschijnlijk een elektron krijgt om een stabiel octet in zijn buitenste schaal te bereiken. Deze neiging is de reden waarom chloor een sterk oxidatiemiddel is.
 Ontwikkelingslanden worden geconfronteerd met stijgende betalingen als gevolg van klimaatverandering, zegt verslag
Ontwikkelingslanden worden geconfronteerd met stijgende betalingen als gevolg van klimaatverandering, zegt verslag Het lozen van waswater in de Oostzee is verantwoordelijk voor honderden miljoenen kosten
Het lozen van waswater in de Oostzee is verantwoordelijk voor honderden miljoenen kosten  Klimaatverandering verantwoordelijk voor warmste winter in Nieuw-Zeeland
Klimaatverandering verantwoordelijk voor warmste winter in Nieuw-Zeeland Waarom zijn planten belangrijk voor mensen en het milieu?
Waarom zijn planten belangrijk voor mensen en het milieu?  Iraakse boeren vechten om vee te redden van droogte
Iraakse boeren vechten om vee te redden van droogte
Hoofdlijnen
- CT-scans laten zien waarom kantelende bomen betere biobrandstof produceren
- Volgens Charles Darwin zal een organisme dat goed geschikt is zijn omgeving waarschijnlijker genen zijn bij de volgende generatie, dit idee vormt basis. Welke theorie?
- Verander je geliefde in een boom met Bios Urn
- Wat is een Sphyillis?
- Onderzoekers verduidelijken hoe cellen zichzelf verdedigen tegen virussen
- Onderzoek schetst hoe sekseverschillen zijn geëvolueerd
- Hoe worden twee soorten cellen genoemd?
- Wat is de studie van cellen afgeworpen van het epitheeloppervlak?
- Wat is de inhoud van de cel?
- Ingenieurs vinden dat antioxidanten de visualisatie van polymeren op nanoschaal verbeteren

- Handheld DNA-sequencers zijn veelbelovend voor het monitoren van microben tijdens voedselproductie

- Wat zit er in deze plant? Het beste geautomatiseerde systeem voor het vinden van potentiële medicijnen

- De eigenschappen van een nieuwe klasse brillen voorspellen
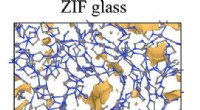
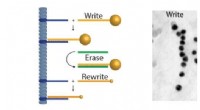
- DNA als supramoleculaire bouwsteen
 Hoe algebraïsche vergelijkingen op te lossen met dubbele exponenten
Hoe algebraïsche vergelijkingen op te lossen met dubbele exponenten Welke verbinding creëert koolstofwaterstof en zuurstof?
Welke verbinding creëert koolstofwaterstof en zuurstof?  Hoe bereid je 0,1 M natriumacetaat?
Hoe bereid je 0,1 M natriumacetaat?  Geen misverstand over Australische steak – food agility-project pakt voedselfraude aan
Geen misverstand over Australische steak – food agility-project pakt voedselfraude aan Wat is de chemische formule en het oxidatiegetal van elk ion in de eerste seconde van de verbinding?
Wat is de chemische formule en het oxidatiegetal van elk ion in de eerste seconde van de verbinding?  Uit de kast komen op je werk is geen eenmalige gebeurtenis
Uit de kast komen op je werk is geen eenmalige gebeurtenis Studenten graven in data-archief en vinden mysterieuze röntgenbron
Studenten graven in data-archief en vinden mysterieuze röntgenbron Behandeling van zonnecelmaterialen onthult vorming van onverwachte microstructuren
Behandeling van zonnecelmaterialen onthult vorming van onverwachte microstructuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

