
Wetenschap
Waarom is puur water neutraal ondanks het feit dat de productie van waterstofionen en hydroxide -ionen?
`` `
2 h₂o ⇌ h₃o + + oh-
`` `
De dubbele pijl geeft aan dat de reactie omkeerbaar is , wat betekent dat het in beide richtingen gaat. Bij evenwicht is de snelheid van de voorwaartse reactie (vorming van H₃o+ en OH-) gelijk aan de snelheid van de omgekeerde reactie (vorming van twee watermoleculen).
Dus waarom is puur water neutraal? Het is omdat de concentraties van H+ en OH-ionen gelijk zijn .
In zuiver water is de concentratie van zowel H+ als OH- 1 x 10^-7 mol per liter , die overeenkomt met een pH van 7.
Dit is de reden waarom gelijke concentraties leiden tot neutraliteit:
* pH -schaal: De pH -schaal meet de zuurgraad of alkaliteit van een oplossing. Een pH van 7 wordt als neutraal beschouwd, onder de 7 is zuur en boven 7 is alkalisch (basic).
* H+ en OH-balans: De zuurgraad wordt bepaald door de concentratie van H+ -ionen, terwijl alkaliteit wordt bepaald door de concentratie van OH-ionen.
* neutralisatie: Wanneer de concentraties van H+ en OH- gelijk zijn, neutraliseren ze elkaar effectief, wat resulteert in een neutrale pH.
Samenvattend:
Terwijl puur water autoionisatie ondergaat, leiden de gelijke concentraties van H+ en OH-ionen geproduceerde, leiden tot een neutrale pH. Het is een evenwicht tussen de vorming en recombinatie van deze ionen die puur water neutraal houdt.
 Aanpassingen van apen voor de Jungle
Aanpassingen van apen voor de Jungle Hoe beïnvloeden behoeften en wensen natuurlijke hulpbronnen?
Hoe beïnvloeden behoeften en wensen natuurlijke hulpbronnen?  Bedrijven sleutel tot het redden van de natuur, zegt WWF-chef
Bedrijven sleutel tot het redden van de natuur, zegt WWF-chef De vorming van een supersterke Mongoolse cycloon en de bijdragende factoren
De vorming van een supersterke Mongoolse cycloon en de bijdragende factoren Onderzoekers ontdekken nieuwe rol voor vreemde organismen in oceaanvoedselweb
Onderzoekers ontdekken nieuwe rol voor vreemde organismen in oceaanvoedselweb
Hoofdlijnen
- Wat doodde de dinosaurussen?
- Hoe erfelijke ziekten werken
- Welk doel hebben vreemd gevormde cellen?
- Hoe analyseren wetenschappers gegevens die ze verzamelen?
- Mummies buikjes om de evolutie van de spijsvertering te onthullen
- De functies van de linker temporale kwab
- Onderzoek onderzoekt hoe druivenplagen bessen opsnuiven
- Van welke cel is insuline afgeleid?
- De ontdekking van cellen is het meest direct gekoppeld van de ontwikkeling de?
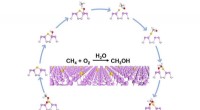
- Goud-fosfor-nanobladen katalyseren selectief aardgas tot groenere energie
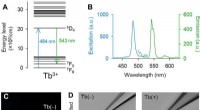
- Met terbium (III) gedoteerd fluorescerend glas voor biomedisch onderzoek
- Efficiënte depolymerisatie in vaste toestand van PET-afval

- Eiwit-gemodificeerde vaste elektrolyt interfase vorming en evolutie in Li-metaalbatterijen

- Hoe bacteriën mangaanoxide nanodeeltjes produceren

 Is koolstof een verbinding of een element?
Is koolstof een verbinding of een element?  Waarom wordt zonne -energie als niet schadelijk beschouwd als het milieu?
Waarom wordt zonne -energie als niet schadelijk beschouwd als het milieu?  Cellen zijn de basiseenheid van levensvirussen op veel belangrijke manieren van cellen, wat is een kenmerkvirussen maar geen cellen?
Cellen zijn de basiseenheid van levensvirussen op veel belangrijke manieren van cellen, wat is een kenmerkvirussen maar geen cellen?  Moeilijk om een Rubiks-kubus op te lossen? Probeer de adaptieve toolbox-theorie over rationaliteit
Moeilijk om een Rubiks-kubus op te lossen? Probeer de adaptieve toolbox-theorie over rationaliteit Moet u de telefoon van uw kind controleren? Hoe weet je wanneer je kind klaar is voor ‘telefoonprivacy’
Moet u de telefoon van uw kind controleren? Hoe weet je wanneer je kind klaar is voor ‘telefoonprivacy’  Wat is het verschil tussen zand- en vuilgrond?
Wat is het verschil tussen zand- en vuilgrond?  Reflecteren de sterren Suns Light?
Reflecteren de sterren Suns Light?  Waar is Constellation?
Waar is Constellation?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

