
Wetenschap
Welke eigenschap van water laat het zoveel verbindingen oplossen?
Dit is waarom:
* Water is een polair molecuul: Dit betekent dat het een enigszins positief uiteinde (waterstofzijde) en een enigszins negatief uiteinde (zuurstofzijde) heeft als gevolg van de ongelijke delen van elektronen in de H-O-binding.
* aantrekkingskracht op ionen en polaire moleculen: Het positieve uiteinde van een watermolecuul wordt aangetrokken tot negatief geladen ionen en het negatieve uiteinde wordt aangetrokken tot positief geladen ionen. Deze attractie helpt om ionische verbindingen uit elkaar te breken en op te lossen. Evenzo kunnen watermoleculen waterstofbruggen vormen met andere polaire moleculen, waardoor hun structuur wordt verstoord en tot oplossing leiden.
Samenvattend: De polariteit van het water maakt het een uitstekend oplosmiddel omdat het een breed scala aan stoffen kan interageren en uit elkaar kan trekken, waaronder ionische verbindingen, polaire moleculen en zelfs sommige niet-polaire moleculen.
 Hoeveel valentie -elektronen zijn er in het polyatomische ionen HPO4 -2?
Hoeveel valentie -elektronen zijn er in het polyatomische ionen HPO4 -2?  Scheiden zwavel en suiker van een mengsel?
Scheiden zwavel en suiker van een mengsel?  Wat is de volgorde van stappen waarmee grote voedingsmoleculen worden opgesplitst in hun respectieve bouwstenalytische enzymen in hydrolysereacties die worden genoemd?
Wat is de volgorde van stappen waarmee grote voedingsmoleculen worden opgesplitst in hun respectieve bouwstenalytische enzymen in hydrolysereacties die worden genoemd?  Chemici hebben verbindingen gemaakt die glaucoom kunnen behandelen
Chemici hebben verbindingen gemaakt die glaucoom kunnen behandelen Hoeveel atomen bevat 0,5 kg natrium?
Hoeveel atomen bevat 0,5 kg natrium?
 Informatie hiaat tussen bijsnijden vullen
Informatie hiaat tussen bijsnijden vullen Studie laat zien hoe je aardgas kunt produceren terwijl je koolstofdioxide opslaat
Studie laat zien hoe je aardgas kunt produceren terwijl je koolstofdioxide opslaat ReNature lanceert nieuwe toolkit voor op de natuur gebaseerde oplossingen
ReNature lanceert nieuwe toolkit voor op de natuur gebaseerde oplossingen Klimaatverandering stelt de drinkwatervoorziening voor nieuwe uitdagingen
Klimaatverandering stelt de drinkwatervoorziening voor nieuwe uitdagingen Onderwaterrobots helpen voorspellen hoe en wanneer ijsplaten instorten
Onderwaterrobots helpen voorspellen hoe en wanneer ijsplaten instorten
Hoofdlijnen
- Organismen die de energie in zonlicht veranderen in voedsel worden genoemd?
- Een schakelaar voor de interne klok:onderzoek naar kwantumbiologie voor nieuwe medische therapieën
- Voorbeeld van dingen die producten wetenschap zijn?
- Voorbeeld van oorzaak en gevolghypothese?
- Hoe drinkt schimmels?
- Wat zijn de chromosomen van het vrouwelijke geslacht in genetica?
- Wat is de term voor ouderorganismen die zijn gekoppeld?
- Wat is een wetenschappelijke spalk?
- Getoonde chimpansees die spontaan om de beurt een cijferpuzzel oplossen
- Op bladeren geïnspireerd oppervlak voorkomt vorstvorming

- Modificatie en degradatie van op Ni-rijke kathode gebaseerde Li-ion-batterijen

- Een gepatenteerde oplossing voor het verlichten van droge mond en de ontwikkeling van voedingsproducten
- Een zwaargewicht oplossing voor lichtere gevechtsvoertuigen

- Van overvloedige koolwaterstoffen tot zeldzame spinvloeistoffen
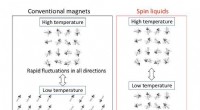
 Hoe Flintlock-pistolen werken
Hoe Flintlock-pistolen werken  Technologieën ontwikkelen die op licht werken
Technologieën ontwikkelen die op licht werken Hoe draagt de zon bij aan het klimaat?
Hoe draagt de zon bij aan het klimaat?  Jim Rossman:We hebben je nieuwe favoriete gadgets gevonden, inclusief een handige manier om sleutels en gereedschap mee te nemen
Jim Rossman:We hebben je nieuwe favoriete gadgets gevonden, inclusief een handige manier om sleutels en gereedschap mee te nemen Eenmalige gelduitgifte van de overheid niet genoeg om arme gezinnen te helpen
Eenmalige gelduitgifte van de overheid niet genoeg om arme gezinnen te helpen Waarom heeft het object met minder massa een grotere versnelling?
Waarom heeft het object met minder massa een grotere versnelling?  Een eendimensionale vloeibare nanogenerator om elektriciteit uit de bloedbaan te halen
Een eendimensionale vloeibare nanogenerator om elektriciteit uit de bloedbaan te halen De belangrijkste biotische en abiotische componenten van het ecosysteem van het Great Barrier Reef
De belangrijkste biotische en abiotische componenten van het ecosysteem van het Great Barrier Reef
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

