
Wetenschap
Hoe beïnvloedt de temperatuur de oplosbaarheid van een opgeloste stof in oplosmiddel?
Endothermische oplossing:
* Verhogende temperatuur verhoogt de oplosbaarheid: Wanneer het oplossingsproces warmte absorbeert (endotherm), biedt het verhogen van de temperatuur de energie die nodig is om de bindingen tussen opgeloste deeltjes te verbreken en de energiebarrière voor het oplossen te overwinnen. Dit leidt tot een toename van de oplosbaarheid.
* Voorbeelden:
* vaste opgeloste stoffen in vloeistoffen: De meeste ionische vaste stoffen en sommige moleculaire vaste stoffen (zoals suiker) lossen gemakkelijker op in vloeistoffen naarmate de temperatuur toeneemt.
* gassen in vloeistoffen: Gassen worden minder oplosbaar in vloeistoffen naarmate de temperatuur toeneemt. Dit komt omdat de verhoogde thermische energie ervoor zorgt dat de gasmoleculen loskomen van de vloeistof en ontsnappen in de atmosfeer.
Exotherme ontbinding:
* Verhogende temperatuur verlaagt de oplosbaarheid: Wanneer het oplossingsproces warmte vrijgeeft (exotherme), verschuift de toenemende temperatuur het evenwicht naar de niet -opgeloste toestand. Dit komt omdat het toevoegen van warmte aan een systeem dat al warmte vrijgeeft, de omgekeerde reactie (neerslag) bevordert.
* Voorbeelden:
* Sommige zouten, zoals calciumsulfaat (CASO4), worden minder oplosbaar in water naarmate de temperatuur toeneemt.
generalisaties en uitzonderingen:
* vaste stoffen in vloeistoffen: Over het algemeen neemt de oplosbaarheid van vaste stoffen in vloeistoffen toe met toenemende temperatuur.
* gassen in vloeistoffen: De oplosbaarheid van gassen in vloeistoffen neemt meestal af met toenemende temperatuur.
* Uitzonderingen: Er zijn enkele uitzonderingen op deze algemene trends. De oplosbaarheid van sommige gassen in water neemt bijvoorbeeld enigszins toe met de temperatuur. Dit komt door de vorming van zwakke interacties tussen de gasmoleculen en watermoleculen.
Factoren die de oplosbaarheid beïnvloeden:
* Aard van de opgeloste stof en oplosmiddel: Polaire opgeloste stoffen lost op in polaire oplosmiddelen (zoals water), en niet -polaire opgeloste stoffen lost op in niet -polaire oplosmiddelen (zoals olie).
* Druk: Druk speelt een belangrijke rol in de oplosbaarheid van gassen in vloeistoffen. De wet van Henry beschrijft deze relatie.
Samenvattend:
Temperatuur beïnvloedt de oplosbaarheid aanzienlijk en de richting van het effect hangt af van of het oplossingsproces endotherme of exotherme is. Het begrijpen van deze relatie is cruciaal in veel toepassingen, waaronder chemische reacties, milieustudies en industriële processen.
 Welk type binding zit in calciumhydroxide?
Welk type binding zit in calciumhydroxide?  Bio-geïnspireerde materialen tonen potentieel voor beschermende uitrusting en textiel
Bio-geïnspireerde materialen tonen potentieel voor beschermende uitrusting en textiel  Welke mineralen zitten er in een bureau?
Welke mineralen zitten er in een bureau?  Wat is het theoretische percentage zink in een monster jodide?
Wat is het theoretische percentage zink in een monster jodide?  Wat is de formule voor ionische verbinding gevormd tussen natrium en jodium?
Wat is de formule voor ionische verbinding gevormd tussen natrium en jodium?
Hoofdlijnen
- Wat is de term voor een paddestoelachtige groei die zich uitstrekt op een stengel van het oppervlak van het slijmmembraan?
- Hoe stadia van mitose in een cel onder een microscoop te identificeren
- Wat is de meest voorkomende witte cel in de granulocytische serie?
- Hoe bieden embryo's bewijs van evolutie?
- Wetenschappers laten zien hoe vrouwelijke gameten het herstel van de bevruchting in bloeiende planten regelen
- Gebruikt cellulaire ademhaling NADPH als zijn elektronendrager?
- Maakt religie een verschil in de politiek?
- Hoe het toevoegen van groene thee-extract aan bereid voedsel het risico op norovirus kan verminderen
- Studie werpt licht op hoe scramblase-eiwitten celmembranen herschikken
- Herbestemming van dimethyloxalylglycine om het glutaminemetabolisme te remmen
- Onderzoeker ontwikkelt duurzaam leeralternatief op basis van groene thee

- Kunstmatige intelligentie ontmoet materiaalwetenschap

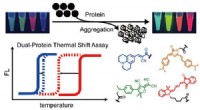
- Onderzoekers kwantificeren thermodynamisch samenspel tijdens co-aggregatie van eiwitten
- Hoe inktviscamouflage huidkanker bij mensen kan helpen voorkomen

 Wat is de energietransformatie in een handlamp met de hand?
Wat is de energietransformatie in een handlamp met de hand?  Piper J-3 Cub
Piper J-3 Cub  Berging Titanic:het terugvinden van de scheepsradio kan een ramp betekenen voor het cultureel erfgoed onder water
Berging Titanic:het terugvinden van de scheepsradio kan een ramp betekenen voor het cultureel erfgoed onder water Zullen de VS het gebruik van plastic voor eenmalig gebruik verbieden, zoals Engeland, India, Hong Kong en andere landen?
Zullen de VS het gebruik van plastic voor eenmalig gebruik verbieden, zoals Engeland, India, Hong Kong en andere landen?  Onderzoeker doet ontdekking van diepzeekoraalriffen in de diepten van de Noord-Pacific
Onderzoeker doet ontdekking van diepzeekoraalriffen in de diepten van de Noord-Pacific Wat betekent de maateenheid voor MF?
Wat betekent de maateenheid voor MF?  Kenmerken van geofysische turbulentie op submesoschaal
Kenmerken van geofysische turbulentie op submesoschaal Wat zijn Double Angle Identities?
Wat zijn Double Angle Identities?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

