
Wetenschap
Reactie van waterstofchloridegas met water?
Hier is een uitsplitsing:
* De reactie:
HCl (G) + H₂o (L) → H₃o⁺ (aq) + Cl⁻ (aq)
* Verklaring:
* hcl is een sterk zuur, wat betekent dat het gemakkelijk een proton doneert (H⁺).
* h₂o Fungeert als basis en accepteert het proton.
* h₃o⁺ is het hydroniumion, een gehydrateerd proton, gevormd wanneer het proton van HCl bindt met een watermolecuul.
* Cl⁻ is het chloride -ion, het resterende deel van het HCL -molecuul.
* Sleutelpunten:
* Deze reactie is zeer exotherme , wat betekent dat het warmte vrijgeeft.
* De resulterende oplossing is zuur , omdat de aanwezigheid van hydroniumionen (H₃o⁺) de pH verlaagt.
* De reactie is onomkeerbaar onder normale omstandigheden.
* Praktische toepassingen:
* Deze reactie is de basis voor de productie van zoutzuur (HCl (aq)) , een zeer belangrijke industriële chemische stof die in tal van toepassingen wordt gebruikt, waaronder:
* Productie van kunststoffen, meststoffen en geneesmiddelen
* Metaalverwerking
* Schoonmaken en sanitaire voorzieningen
* Voedselverwerking
Samenvattend produceert de reactie van waterstofchloridegas met water zoutzuur, een sterk zuur dat een belangrijke rol speelt in verschillende industriële en wetenschappelijke toepassingen.
 De rol van dammen bij het verminderen van de wereldwijde blootstelling aan overstromingen onder klimaatverandering
De rol van dammen bij het verminderen van de wereldwijde blootstelling aan overstromingen onder klimaatverandering Enorme vulkaanuitbarsting veroorzaakte 140 miljoen jaar geleden geen klimaatverandering en massale uitsterving
Enorme vulkaanuitbarsting veroorzaakte 140 miljoen jaar geleden geen klimaatverandering en massale uitsterving Beschrijf de sfeer bovenop een berg?
Beschrijf de sfeer bovenop een berg?  Wat is bosgrond?
Wat is bosgrond?  Tuinwormen en klimaatverandering ondermijnen natuurlijke kustbescherming
Tuinwormen en klimaatverandering ondermijnen natuurlijke kustbescherming
Hoofdlijnen
- Vroegtijdige waarschuwing gezondheids- en welzijnssysteem kan boeren miljoenen ponden besparen
- Wat is de celtheor?
- Hoe een cel te splitsen in Two
- Wat zijn de twee hoofdcomponenten van een immuunrespons?
- Welke woorden kunt u gebruiken om een hypothese te vormen?
- Wat is kwantitave onherkenning in het genen?
- Wat is het geleidende celtype in Phloem?
- Fermentatie treedt op wanneer een cel wordt?
- Waarom enzymen zijn eiwitten?
- Onderzoekers verbeteren de beschrijving van defecte oxiden met de eerste principes-berekening
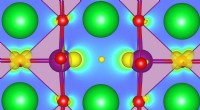
- Gasmaskerfilters bestuderen zodat mensen gemakkelijker kunnen ademen

- Biochemici onthullen moleculair mechanisme voor regulatie van motoreiwitten
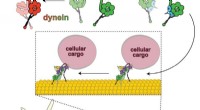
- Onderzoekers schetsen de huidige stand van zaken in de technologie van kalium-ionbatterijen
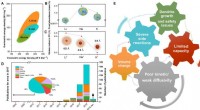
- Wetenschappers onthullen hoe wasmiddelen eigenlijk werken
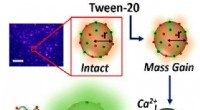
 Waarom is argon zeer stabiel en niet reactief?
Waarom is argon zeer stabiel en niet reactief?  Wat zijn enkele technologische vooruitgang in de wetenschap?
Wat zijn enkele technologische vooruitgang in de wetenschap?  Hoe de zaden van planeten vorm krijgen
Hoe de zaden van planeten vorm krijgen Welke eigenschappen van staal maken het bruikbaarder dan krijt?
Welke eigenschappen van staal maken het bruikbaarder dan krijt?  Hoe DNA-reparatie kanker helpt voorkomen
Hoe DNA-reparatie kanker helpt voorkomen  Welke chemische reacties is het type chemicaliën dat wordt verbroken?
Welke chemische reacties is het type chemicaliën dat wordt verbroken?  Is Germanium een goede elektriciteitsgeleider?
Is Germanium een goede elektriciteitsgeleider?  Herziening van historische voorraadroutes kan zeldzame stukken inheemse planten en dieren in gevaar brengen
Herziening van historische voorraadroutes kan zeldzame stukken inheemse planten en dieren in gevaar brengen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

