
Wetenschap
Als een atoom van zwavel mocht reageren met atomen waterstof welke de moleculen zouden worden gevormd?
Als een atoom van zwavel mocht reageren met atomen van waterstof, het molecuul waterstofsulfide (H₂s) zou worden gevormd.
Dit is waarom:
* zwavel (s) heeft zes valentie -elektronen (elektronen in de buitenste schaal). Het heeft nog twee elektronen nodig om een stabiel octet te bereiken.
* waterstof (h) Heeft één valentie -elektron. Het heeft nog een elektron nodig om een stabiel duet te bereiken.
Om stabiliteit te bereiken, kan één zwavelatoom zijn elektronen delen met twee waterstofatomen. Dit resulteert in de vorming van een covalente binding tussen de zwavel en elk waterstofatoom, waardoor het molecuul H₂s ontstaat .
Hoofdlijnen
- Geef de haaien niet de schuld:uit onderzoek blijkt waarom er steeds meer gehaakte tarpoenen worden gegeten
- Dance-gerelateerde wetenschapsprojecten
- Welk deel van een nucleïnezuur maakt het mogelijk om vormcode (2 punt) te worden gebruikt?
- Hoe denken wetenschappers dat het eerste meercellige organisme is ontstaan?
- Wat is het katalyserende metabole reacties in cellen?
- Welk molecuul is in de eerste plaats verantwoordelijk voor de verschillen van cellen?
- Waarom is water belangrijk in cella?
- Wat is de verzameling koolhydraatgroepen op een menselijk extern oppervlak dat wordt genoemd?
- Waarom hebben cellen fosfor nodig?
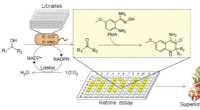
- Nieuwe high-throughput screeningmethode ontwikkeld voor ketonen
- Onderzoekers ontwikkelen tool voor snelle diagnose van bacteriële infecties

- Ongeneeslijke ziekten krijgen een nieuw hulpmiddel voor het ontdekken van RNA-geneesmiddelen

- Hydrogel coating is de eerste om ijsvorming op 3 verschillende manieren te voorkomen

- Nieuwe techniek bereidt 2-D perovskiet-eenkristallen voor voor de hoogste fotodetectie

 Toetappende test evalueert valrisico bij Parkinsonpatiënten
Toetappende test evalueert valrisico bij Parkinsonpatiënten  Waar kunt u een waterstofbinding vinden?
Waar kunt u een waterstofbinding vinden?  Hoge variabiliteit is het gevolg van complexe dataworkflows, studie vondsten
Hoge variabiliteit is het gevolg van complexe dataworkflows, studie vondsten Geëlektrificeerde magneten:onderzoekers ontdekken een nieuwe manier om met gegevens om te gaan
Geëlektrificeerde magneten:onderzoekers ontdekken een nieuwe manier om met gegevens om te gaan Wat is chromatografische vloeistof?
Wat is chromatografische vloeistof?  Activiteit om aan te tonen dat water een slechte geleider van warmte is?
Activiteit om aan te tonen dat water een slechte geleider van warmte is?  China moet melk groen maken
China moet melk groen maken NASA vindt Tropical Storm Dolphin aan het zwemmen
NASA vindt Tropical Storm Dolphin aan het zwemmen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


