
Wetenschap
Wat zijn atomen van hetzelfde element dan hebben verschillende atoommassa's?
Hier is een uitsplitsing:
* element: Een pure stof bestaande uit slechts één type atoom. Alle atomen van een bepaald element hebben hetzelfde aantal protonen (het atoomnummer van het element definiëren).
* Atomische massa: De totale massa van een atoom, voornamelijk bepaald door het aantal protonen en neutronen in zijn kern.
* isotopen: Atomen van hetzelfde element met hetzelfde aantal protonen maar verschillende aantallen neutronen. Dit verschil in neutronen resulteert in een andere atoommassa.
Bijvoorbeeld:
* carbon-12 en carbon-14 zijn beide isotopen van koolstof.
* Beide hebben 6 protonen (ze definiëren als koolstof).
* Carbon-12 heeft 6 neutronen, terwijl koolstof-14 8 neutronen heeft.
* Dit maakt de atoommassa van koolstof-12 12 en de atoommassa van koolstof-14 14.
Isotopen hebben verschillende fysieke eigenschappen, zoals radioactief verval, en kunnen worden gebruikt in verschillende toepassingen zoals:
* Radioactive Dating (Carbon-14 dating)
* medische beeldvorming (Technetium-99m)
* Kankerbehandeling (Cobalt-60)
Laat het me weten als je nog meer vragen hebt!
 Welke vloeistoffen zijn dichter dan niet-water oplosbaar en niet-toxisch in water?
Welke vloeistoffen zijn dichter dan niet-water oplosbaar en niet-toxisch in water?  Wat doet lithiumcarbonaat met je lichaam?
Wat doet lithiumcarbonaat met je lichaam?  Wat zijn de oxiden van stikstof?
Wat zijn de oxiden van stikstof?  Leg uit waarom destillatie een goede manier is om C8H18- en C5H12 -vloeistoffen te scheiden?
Leg uit waarom destillatie een goede manier is om C8H18- en C5H12 -vloeistoffen te scheiden?  Tweaking van legeringsmicrochemie voor vlekkeloos 3D-printen van metaal
Tweaking van legeringsmicrochemie voor vlekkeloos 3D-printen van metaal
 Wat is een element van de natuur dat mechanische verwering kan veroorzaken door over rotsen te stromen of mee te nemen in een stroom?
Wat is een element van de natuur dat mechanische verwering kan veroorzaken door over rotsen te stromen of mee te nemen in een stroom?  Nieuw ontdekte diepzeemicroben slokken broeikasgassen op en misschien olielozingen, te
Nieuw ontdekte diepzeemicroben slokken broeikasgassen op en misschien olielozingen, te Hoe redden we bejaarde Australiërs van de hitte? Onze steden groener maken is een goed begin
Hoe redden we bejaarde Australiërs van de hitte? Onze steden groener maken is een goed begin Nieuwe bevindingen over klimaatonderzoek in de koolstofcyclus
Nieuwe bevindingen over klimaatonderzoek in de koolstofcyclus Indonesië stuurt honderden zeecontainers vol afval terug
Indonesië stuurt honderden zeecontainers vol afval terug
Hoofdlijnen
- Hoe bacteriën zich aan cellen hechten:basis voor de ontwikkeling van een nieuwe klasse antibiotica
- In alledaagse spraak gebruiken mensen vaak de term theorie om een voorgevoel of gok te betekenen op basis van voorkennis. Wetenschappers goed geteste verklaring. Wat zou wetenschapper M?
- Wat genereren seksuele reproductiemutatie en kruising in een populatie?
- Wat zijn biotische en antibiotische factoren?
- Hoe orang-oetanmoeders hun kroost helpen bij het leren
- Welke bacteriën leven en krijgen voeding in uw darmen?
- Wetenschappers publiceren nieuw onderzoek naar hoe individuele cellen reageren op virale infecties
- Welk onderdeel van de biosfeer is een voorbeeld organische stof?
- Het kwantumfysica-concept van kritische massa
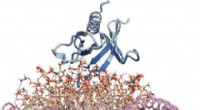
- Inzichten op atoomniveau verkregen voor een belangrijk lipidenbindend eiwit dat betrokken is bij kanker
- Microgolfplastic verlengt de levensduur van lithium-zwavelbatterijen

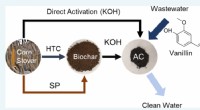
- Schoner water door maïs
- Lab ontwikkelt grafeenelektrode met twee oppervlakken om water te splitsen in waterstof en zuurstof

- Hoe biokatalysatoren onsterfelijk te maken?

 Hoe Nepal profiteert als vrouwen actief worden in waterbeheer
Hoe Nepal profiteert als vrouwen actief worden in waterbeheer Hoe astronauten werken
Hoe astronauten werken  Hoe valbloemen bestuivende voedseldieven aantrekken en misleiden
Hoe valbloemen bestuivende voedseldieven aantrekken en misleiden  Wat is de molaire massa van ammoniumchromaat NH4 2CRO4?
Wat is de molaire massa van ammoniumchromaat NH4 2CRO4?  Terugreactie voor het eerst waargenomen in simulatie van zwart gat in watertanks
Terugreactie voor het eerst waargenomen in simulatie van zwart gat in watertanks Voorbeelden van een recessief allel
Voorbeelden van een recessief allel  Is de kracht van voorstelling en zwaartekracht op een actiereactiepaar van een vliegtuig?
Is de kracht van voorstelling en zwaartekracht op een actiereactiepaar van een vliegtuig?  Enzymconformatie beïnvloedt de prestaties van lipase-aangedreven nanomotoren
Enzymconformatie beïnvloedt de prestaties van lipase-aangedreven nanomotoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

