
Wetenschap
Welke van deze stoffen heeft het hoogste smeltpunt Alcl3 NaCl KCL of RBCL?
Inzicht in smeltpunt
Smeltpunt is de temperatuur waarbij een vaste overgangen in een vloeistof. De sterkte van de krachten die de deeltjes bij elkaar houden in de vaste toestand bepaalt het smeltpunt. Sterkere krachten vereisen meer energie (hogere temperatuur) om te breken.
ionische verbindingen en smeltpunt
De verbindingen die u hebt vermeld, zijn allemaal ionische verbindingen. De sterkte van de ionische binding, die de elektrostatische aantrekkingskracht is tussen tegengesteld geladen ionen, bepaalt het smeltpunt. Dit is hoe de factoren die de kracht van ionische binding beïnvloeden van toepassing zijn op uw lijst:
* opladen: Hogere ladingen op de ionen leiden tot sterkere attracties.
* Grootte: Kleinere ionen hebben een grotere ladingsdichtheid, wat leidt tot sterkere attracties.
het vergelijken van de verbindingen
* alcl3: Aluminium heeft een +3 lading en chloor heeft een -1 lading. ALCL3 heeft echter een meer covalent karakter vanwege het grootteverschil tussen de ionen.
* NaCl: Natrium heeft een +1 lading en chloor heeft een -1 lading.
* KCL: Kalium heeft een +1 lading en chloor heeft een -1 lading. Kalium is groter dan natrium.
* rbcl: Rubidium heeft een +1 lading en chloor heeft een -1 lading. Rubidium is groter dan kalium.
Conclusie
Op basis van de bovenstaande factoren heeft NaCl het hoogste smeltpunt. Dit is waarom:
* opladen: Alle vier verbindingen hebben dezelfde grootte van lading (+1 en -1).
* Grootte: Natrium- en chloorionen zijn kleiner dan kalium en chloor, en zelfs kleiner dan rubidium en chloor. Kleinere ionen hebben sterkere attracties.
Daarom zal NaCl het hoogste smeltpunt hebben gevolgd door KCL, RBCL en vervolgens ALCL3.
 Plastics van de toekomst zullen vele vorige levens leiden, dankzij chemische recycling
Plastics van de toekomst zullen vele vorige levens leiden, dankzij chemische recycling Wat is de formulemassa voor ammoniumion?
Wat is de formulemassa voor ammoniumion?  Hoe platina is zeer plooibaar is, slechts één gram ervan kan in een draad worden uitgerekt met welke lengte?
Hoe platina is zeer plooibaar is, slechts één gram ervan kan in een draad worden uitgerekt met welke lengte?  Aerogel geïntegreerd hout biedt betere isolatie dan bestaande materialen op plasticbasis
Aerogel geïntegreerd hout biedt betere isolatie dan bestaande materialen op plasticbasis Steen malen in poeder
Steen malen in poeder
 Wat betekent dit citaat wanneer de wetenschap een ontdekking doet, grijpt de duivel het terwijl engelen over de beste manier debatteren om het te gebruiken?
Wat betekent dit citaat wanneer de wetenschap een ontdekking doet, grijpt de duivel het terwijl engelen over de beste manier debatteren om het te gebruiken?  Onderzoek naar de betekenis van oude geometrische grondwerken in het zuidwesten van Amazonië
Onderzoek naar de betekenis van oude geometrische grondwerken in het zuidwesten van Amazonië Gevangenisstraffen voor Franse oplichters in koolstofhandel
Gevangenisstraffen voor Franse oplichters in koolstofhandel De diverse fysieke kenmerken van land hebben een enorme ontwikkeling van toekomstige mogelijkheden waarom?
De diverse fysieke kenmerken van land hebben een enorme ontwikkeling van toekomstige mogelijkheden waarom?  COVID-19 maakt luchtvervuiling wereldwijd een topprioriteit:rapport
COVID-19 maakt luchtvervuiling wereldwijd een topprioriteit:rapport
Hoofdlijnen
- Wat veroorzaakt het uitsterven van planten en dieren?
- Nieuwe oude dolfijnsoort Urkudelphis chawpipacha ontdekt in Ecuador
- Wat is biologische besmetting die voortvloeit uit weersomstandigheden?
- De verjaardag van inktvissen beïnvloedt de paring:mannelijke speerinktvissen blijken sneakers of consorten te worden, afhankelijk van de geboortedatum
- Hoe kan een fabriek schadelijk zijn voor de levende organismen?
- Hoe heet een wetenschapper die planten bestudeert?
- Waarom vertonen sommige menselijke eigenschappen een groot aantal fenotypes?
- Mutante cellen die op de een of andere manier geen DNA kunnen kopiëren, blijven zich delen terwijl dat niet zou moeten, met rampzalige gevolgen
- Hoe melkveehouders zich kunnen aanpassen aan klimaatverandering
- Chemicus stelt nieuwe methode voor voor het synthetiseren van voorlopers voor Parkinson-medicijnen
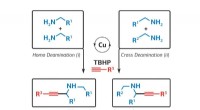
- Maïsvelden kunnen een rol spelen bij het recyclen van oude elektronica

- Kan een hightech snuffelaar ons helpen beschermen?

- Techniek om tweecomponenten biologische sensoren te finetunen
- Potentiële testartefacten bij antimalariascreening

 Wat is de relatie tussen tijdsperiode en snelheid in circulaire beweging?
Wat is de relatie tussen tijdsperiode en snelheid in circulaire beweging?  Weet je iets over wetenschap?
Weet je iets over wetenschap?  Wat is de Apollo en heeft het ooit Moon bereikt?
Wat is de Apollo en heeft het ooit Moon bereikt?  NASA-beheerder legt uit dat Twitter met SpaceX heeft gekletst
NASA-beheerder legt uit dat Twitter met SpaceX heeft gekletst Welke rots absorbeert waterkorrelige rotsen of kristallen rotsen?
Welke rots absorbeert waterkorrelige rotsen of kristallen rotsen?  Een duidelijker beeld geven van het volledige potentieel van nanotechnologieën
Een duidelijker beeld geven van het volledige potentieel van nanotechnologieën Wat zijn de vijf middelgrote sterren?
Wat zijn de vijf middelgrote sterren?  Klimaatvriendelijke koeling kan de uitstoot van broeikasgassen terugdringen en miljarden besparen:UN
Klimaatvriendelijke koeling kan de uitstoot van broeikasgassen terugdringen en miljarden besparen:UN
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

