
Wetenschap
Welke stoffen vormen elektrische stroom door water?
Dit is waarom:
* zouten: Wanneer zouten oplossen in water, dissociëren ze zich in hun samenstellende ionen. Tafelzout (NaCl) lost bijvoorbeeld op in natriumionen (Na+) en chloride-ionen (Cl-). Deze ionen zijn vrij om te bewegen, waardoor elektriciteit kan stromen.
* zuren: Zuren geven waterstofionen (H+) vrij wanneer opgelost in water. Deze ionen kunnen een elektrische stroom dragen.
* Bases: Bases geven hydroxide-ionen vrij (OH-) wanneer opgelost in water. Deze ionen kunnen ook een elektrische stroom dragen.
Daarom zijn de stoffen waarmee elektrische stroom door water kan passeren:
* opgeloste zouten
* zuren
* bases
Het is belangrijk op te merken dat zelfs een kleine hoeveelheid onzuiverheden de geleidbaarheid van water aanzienlijk kan vergroten. Daarom is het gevaarlijk om in de buurt van water te zijn tijdens een elektrische storm of om elektrische apparaten met natte handen aan te kunnen.
 Wat houdt massale uitstervingen tegen? Lessen uit de afsterving van amfibieën in Panama
Wat houdt massale uitstervingen tegen? Lessen uit de afsterving van amfibieën in Panama  Energie die wordt losgelaten door onderzeese vulkanen kan een continent van stroom voorzien
Energie die wordt losgelaten door onderzeese vulkanen kan een continent van stroom voorzien Giftige PAK-luchtverontreinigende stoffen uit fossiele brandstoffen vermenigvuldigen zich in zonlicht
Giftige PAK-luchtverontreinigende stoffen uit fossiele brandstoffen vermenigvuldigen zich in zonlicht Lavas in het laboratorium kan mijnwerkers naar nieuwe ijzerertsafzettingen leiden
Lavas in het laboratorium kan mijnwerkers naar nieuwe ijzerertsafzettingen leiden Wetenschappers waarschuwen dat zoute meren wereldwijd in erbarmelijke situatie verkeren
Wetenschappers waarschuwen dat zoute meren wereldwijd in erbarmelijke situatie verkeren
Hoofdlijnen
- Welke structuren zijn gebruikelijk voor zowel broekcellen als dierencellen?
- Wat voor soort kruis is het toen een eigenschap doorgaat met de sekschromosomen?
- Zeeslakken weten hoe ze hun huisvestingskosten moeten begroten
- Wat zijn de meest efficiënte biomoleculen voor het opslaan van energie. Zou het vetten nucleïnezuren zijn koolhydraten of eiwitten?
- Hoeveel chromosomen zijn er in een dandilion?
- Wat scheidt de DNA -strengen tijdens replicatie?
- Wat is een andere naam voor lichtafhankelijke reaties van fotosynthese?
- Waarom leven vrouwen langer dan mannen?
- Wat zijn drie primaire categorieën waarin voedselmoleculen vallen?
- 2D-materialen tot het uiterste brengen
- Nieuwe goedkope en niet-toxische methode voor het maken van benzeenringen

- Nanocilindervibraties helpen bij het kwantificeren van polymeeruitharding voor 3D-printen
- De eerste mechanosynthese van een moleculair kristal met een Borromeaanse topologie

- Katalysatoren zoals een pincet gebruiken om één enantiomeer uit een gespiegeld paar te selecteren
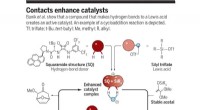
 Europese tornado's vormen een niet-erkende bedreiging, zeggen Britse meteorologen
Europese tornado's vormen een niet-erkende bedreiging, zeggen Britse meteorologen $ 169 miljard voor 29, 000 levens? Studie berekent kosten van Amerikaanse shutdowns
$ 169 miljard voor 29, 000 levens? Studie berekent kosten van Amerikaanse shutdowns In-ear siliconen speakers voor internet of voice
In-ear siliconen speakers voor internet of voice Zoals de hond van Pavlov, deze thermoplast leert een nieuwe truc:lopen
Zoals de hond van Pavlov, deze thermoplast leert een nieuwe truc:lopen Wat zal GLAST ons vertellen?
Wat zal GLAST ons vertellen?  Wat zijn de eigenschappen van radiatorvloeistof en wat zijn vloeistoffen in radiatoren?
Wat zijn de eigenschappen van radiatorvloeistof en wat zijn vloeistoffen in radiatoren?  Een betere batterij bouwen, laag voor laag
Een betere batterij bouwen, laag voor laag Amazon zegt dat sommige e-mailadressen van klanten zijn vrijgegeven
Amazon zegt dat sommige e-mailadressen van klanten zijn vrijgegeven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

