
Wetenschap
Ethanoylchloride en waterige zilveren niraat?
Reactievergelijking:
Ch₃cocl (l) + agno₃ (aq) → ch₃co₂ag (aq) + agcl (s) + hno₃ (aq)
Verklaring:
* ethanoylchloride (ch₃cocl) is een reactief acylchloride.
* waterig zilvernitraat (agno₃) Biedt het nitraation (NO₃⁻) en zilverion (Ag⁺).
* zilveren chloride (AGCL) is een wit neerslag dat vormt, wat aangeeft dat de reactie is opgetreden.
* ethaanzuur (ch₃co₂h) is een zwak zuur gevormd als een bijproduct van de reactie.
* salpeterzuur (hno₃) is een sterk zuur dat ook wordt gevormd als een bijproduct.
mechanisme:
De reactie verloopt door een nucleofiel acylsubstitutiemechanisme.
1. Nucleofiele aanval: Het nitraation (NO₃⁻) werkt als een nucleofiel en valt de carbonylkoolstof van ethanoylchloride aan.
2. Verlaten van groepsafwijking: Het chlooratoom, een goede vertragingsgroep, vertrekt van de carbonyl -koolstof en vormt een tetraëdrisch tussenproduct.
3. Protonoverdracht: Een proton wordt overgebracht van het tetraëdrische tussenproduct naar het nitraation, het regenereren van het nitraation en het vormen van ethaanzuur (ch₃co₂h).
4. Vorming van zilver ethanoaat: Het zilverion (Ag⁺) reageert met het ethanoaat -ion (ch₃co₂⁻) om zilveren ethanoaat (ch₃co₂ag) te vormen, die in oplossing blijft.
Over het algemeen resulteert de reactie tussen ethanoylchloride en waterig zilvernitraat in de vorming van zilverchloride -neerslag, zilverethanoaat in oplossing en salpeterzuur.
 Wat is de rol van de zon in fotosynthese?
Wat is de rol van de zon in fotosynthese?  Lightrail-treinen in Salt Lakes zijn speurneuzen van luchtkwaliteit
Lightrail-treinen in Salt Lakes zijn speurneuzen van luchtkwaliteit Zaadmengsels en verzekeringsongediertebestrijding:toekomstige norm in de Corn Belt?
Zaadmengsels en verzekeringsongediertebestrijding:toekomstige norm in de Corn Belt?  Wat veroorzaakt recordoverstromingen en hittegolven in China?
Wat veroorzaakt recordoverstromingen en hittegolven in China? Wetenschappers ziften door maanvuil voor record van vroege aardse gesteenten
Wetenschappers ziften door maanvuil voor record van vroege aardse gesteenten
Hoofdlijnen
- Wat creëerde de eerste levende micro -organismen op aarde?
- 7 soorten bindweefsel
- Tests laten een mooie toekomst zien voor gadonanotubes bij het volgen van stamcellen
- Wat zijn kenmerken van domein archaea?
- Een eiland verkennen dat is binnengevallen door padden en kikkers
- Wat is de massa van een gemiddelde cel?
- Waarom evolutie vaak de voorkeur geeft aan kleine dieren en andere organismen
- Verdeel en definieer:aanwijzingen om te begrijpen hoe stamcellen verschillende soorten produceren
- Worden gameten geproduceerd in meiose identiek aan elkaar, maar anders dan oudercel?
- Actie van geneesmiddelverbindingen in weefsel onthuld door nieuwe techniek
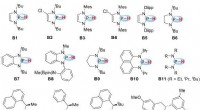
- N-heterocyclische fosfines:veelbelovende katalysatoren voor transferhydrogenering
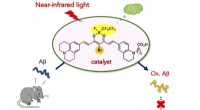
- Nabij-infrarood fotoactiveerbare oxygenatiekatalysatoren van amyloïde peptide
- Een fundamentele tekortkoming in modellen voor luchtvervuiling

- Van compost tot composiet:een milieuvriendelijke manier om rubber te verbeteren

 Een voorwerp dat van een hoogte h valt, bereikt een snelheid van 6 m/s net voordat het de grond raakt, vind waarde h?
Een voorwerp dat van een hoogte h valt, bereikt een snelheid van 6 m/s net voordat het de grond raakt, vind waarde h?  Dolfijnengezondheidscontrole toont toestand van onze oceanen
Dolfijnengezondheidscontrole toont toestand van onze oceanen Wat is de tektonische theorie van de plaat en hoe mogelijk?
Wat is de tektonische theorie van de plaat en hoe mogelijk?  Een klein verband met grote implicaties:op koolstof gebaseerde elektronica bedraden
Een klein verband met grote implicaties:op koolstof gebaseerde elektronica bedraden Hoe koffie werkt
Hoe koffie werkt  Hoe mensen mechanische energie gebruiken?
Hoe mensen mechanische energie gebruiken?  Heeft menselijke geografie en fysiek zich te relateren?
Heeft menselijke geografie en fysiek zich te relateren?  Is scheikunde een harde wetenschap of zachte wetenschap?
Is scheikunde een harde wetenschap of zachte wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

