
Wetenschap
Wanneer worden waterstofbruggen gevormd?
Hier is een uitsplitsing:
Condities voor vorming van waterstofbruggen:
1. Aanwezigheid van een zeer elektronegatief atoom: Zuurstof, stikstof en fluor zijn de meest voorkomende elektronegatieve atomen die betrokken zijn bij waterstofbinding.
2. Covalente binding tussen waterstof en het elektronegatieve atoom: Dit creëert de gedeeltelijke positieve lading op het waterstofatoom.
3. Interactie met een ander elektronegatief atoom: Het gedeeltelijk positieve waterstofatoom wordt aangetrokken tot de alleenstaande paren elektronen op een ander elektronegatief atoom, waardoor de waterstofbinding wordt gevormd.
Voorbeelden van waterstofbinding:
* water (h₂o): Het zuurstofatoom in water trekt de elektronen in de O-H-bindingen aan, waardoor een gedeeltelijke negatieve lading op de zuurstof en een gedeeltelijke positieve lading op de waterstofatomen ontstaat. Deze gedeeltelijke ladingen zorgen voor waterstofbinding tussen watermoleculen.
* DNA: Waterstofbindingen houden de twee DNA -strengen bij elkaar en vormen de dubbele helixstructuur. Deze bindingen worden gevormd tussen stikstofbasen op de twee strengen.
* eiwitten: Waterstofbindingen helpen de driedimensionale structuur van eiwitten te stabiliseren.
Key -kenmerken van waterstofbruggen:
* sterker dan van der Waals krachten, maar zwakker dan covalente bindingen.
* Directioneel van aard: De waterstofbinding wordt gevormd in een specifieke richting, meestal langs de lijn die het waterstofatoom en het elektronegatieve atoom verbindt.
* belangrijk in biologische systemen: Ze spelen cruciale rollen bij het bij elkaar houden van DNA- en eiwitstructuren en bij het beïnvloeden van de eigenschappen van water.
Laat het me weten als je nog meer vragen hebt over waterstofbindingen!
Hoofdlijnen
- Het overbruggen van twee veelvraatpopulaties in Fennoscandia is noodzakelijk voor het behoud
- Zijn er slechts 3 soorten wetenschap?
- Licht werpend op hoe bacteriën met elkaar omgaan
- Welke moleculen zouden de biosynthetische route remmen die leidt tot de vorming van DNA en RNA?
- Waarom zijn mutaties in lichaamscellen geen bron van genetische variatie?
- Identificeren van geschikte vijverlandschappen voor de bescherming van amfibieën
- Vervagende lichten:uitgebreid onderzoek onthult meerdere bedreigingen voor de vuurvliegpopulaties in Noord-Amerika
- Het belang van wetenschappelijke namen voor organismen
- Vroegtijdige waarschuwing gezondheids- en welzijnssysteem kan boeren miljoenen ponden besparen
- Door dik en dun:neutronen volgen lithiumionen in batterij-elektroden

- Superspons belooft effectieve giftige opruiming van meren en meer

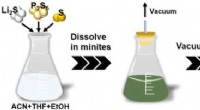
- Ontwikkeling van een nieuwe grootschalige productietechnologie voor sulfide vaste elektrolyten
- Legeronderzoek maakt de weg vrij voor nieuwe materialen

- Nieuw lichtgewicht metaal zo vormbaar als aluminium plaatwerk met 1,5 keer hogere sterkte

 Hoe piramides werken
Hoe piramides werken  Hoeveel stenen zitten er in 161 pond?
Hoeveel stenen zitten er in 161 pond?  Wat is malacologie?
Wat is malacologie?  Berekening van percentagereductie
Berekening van percentagereductie 5 Arduino Projectideeën
5 Arduino Projectideeën  Wat zijn twee of meer stoffen die samen zijn maar niet gecombineerd worden genoemd?
Wat zijn twee of meer stoffen die samen zijn maar niet gecombineerd worden genoemd?  De uitdagingen van een lange ruimtevlucht oplossen met 3D-printen
De uitdagingen van een lange ruimtevlucht oplossen met 3D-printen Als een golf frequentie heeft van 250 Hz en lengte 1,3 meter, wat zijn de snelheidsgeluidsgolven?
Als een golf frequentie heeft van 250 Hz en lengte 1,3 meter, wat zijn de snelheidsgeluidsgolven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


