
Wetenschap
Een monster van 50,0 ml van 0,436 m NH4NO3 wordt verdund met water tot een totaal volume 250,0 Wat de ammoniumnitraatconcentratie in de resulterende oplossing?
Inzicht in verdunning
Verdunning is het proces van het verminderen van de concentratie van een oplossing door meer oplosmiddel toe te voegen (in dit geval water). Het belangrijkste principe is dat de totale hoeveelheid opgeloste stof (ammoniumnitraat) hetzelfde blijft, hoewel het volume toeneemt.
Berekeningen
1. Bereken de mol NH4NO3 in de eerste oplossing:
* Moles =Molarity X Volume (in liters)
* Mol =0,436 m x 0,050 l =0,0218 mol NH4NO3
2. Aangezien de mol NH4NO3 constant blijft, kan de nieuwe concentratie worden berekend met behulp van het uiteindelijke volume:
* Nieuwe molariteit =mol / nieuw volume (in liters)
* Nieuwe molariteit =0,0218 mol / 0,250 L =0,0872 m
Antwoord: De ammoniumnitraatconcentratie in de resulterende oplossing is 0,0872 M.
 De impact van het benoemen van winterstormen
De impact van het benoemen van winterstormen Nieuw inzicht in het Grote Sterven
Nieuw inzicht in het Grote Sterven Waarom zijn mensen zo geïnteresseerd in wetenschap?
Waarom zijn mensen zo geïnteresseerd in wetenschap?  De meerderheid van de berichtgeving over klimaatverandering is nu accuraat:studie
De meerderheid van de berichtgeving over klimaatverandering is nu accuraat:studie Geowetenschappers roepen op tot actie om raciale ongelijkheid in het veld aan te pakken
Geowetenschappers roepen op tot actie om raciale ongelijkheid in het veld aan te pakken
Hoofdlijnen
- Wat zijn enkele goede DNA-wetenschapsprojecten?
- Onderzoekers bepalen hoe mechanische krachten de herkenning en signalering van T-cellen beïnvloeden
- Baseparen in menselijke haploïde cel?
- Wat is een soort fossiel dat geen organisme?
- Wat is de studie van hoe een interne structuur van een organismen functioneert?
- Wat gebruiken chloroplasten om glucose te maken?
- Waarom dassen ten onrechte worden gedemoniseerd en wat we kunnen doen om te helpen
- Hoe sterolen de celdeling in planten beïnvloeden
- Wat is de rol van proteolytische enzymen in de celcyclus?
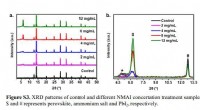
- Efficiënte perovskiet-zonnecellen ontwikkeld door interface-gemedieerde recombinatie te verminderen
- waren heet, vochtige zomers de sleutel tot de oorsprong van het leven?
- Innovatiepioniers scoren wereldprimeur voor duurzaam bouwen met grafeenbeton

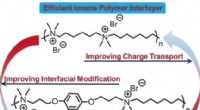
- Fullerenen overbruggen geleidende kloof in organische fotovoltaïsche energie
- Onderzoekers vinden dat de microstructuur van cuttlebones op een goede plek zit

 Recycling van plastic - in Japanse stijl
Recycling van plastic - in Japanse stijl Wat zijn de voorbeelden van copulatieve verbindingen?
Wat zijn de voorbeelden van copulatieve verbindingen?  Waarom denken wetenschappers dat zuurstof zich in de atmosfeer heeft opgebouwd?
Waarom denken wetenschappers dat zuurstof zich in de atmosfeer heeft opgebouwd?  Afbeelding:Zwevend boven Jupiter
Afbeelding:Zwevend boven Jupiter Welke soorten protogalactische wolken vormen het meest waarschijnlijk een elliptisch sterrenstelsel?
Welke soorten protogalactische wolken vormen het meest waarschijnlijk een elliptisch sterrenstelsel?  Wat zou er gebeuren als de aarde zou stoppen met draaien?
Wat zou er gebeuren als de aarde zou stoppen met draaien?  Uit welk deel van een plant komt groenten?
Uit welk deel van een plant komt groenten?  In welk jaar publiceerde Tsiolkovsky het eerste bewijs dat ruimtevaart mogelijk is?
In welk jaar publiceerde Tsiolkovsky het eerste bewijs dat ruimtevaart mogelijk is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

