
Wetenschap
Welk volume zuurstof is nodig om te reageren met een vaste zwavelvorm 3.5L SO2?
1. Schrijf de gebalanceerde chemische vergelijking:
S (s) + o₂ (g) → so₂ (g)
2. Bepaal de molverhouding:
De gebalanceerde vergelijking laat zien dat 1 mol zwavel reageert met 1 mol zuurstof om 1 mol zwaveldioxide te produceren.
3. Pas de wet van Avogadro toe:
De wet van Avogadro stelt dat gelijkwaardige volumes van gassen bij dezelfde temperatuur en druk hetzelfde aantal moleculen (en dus mol) bevatten. Omdat we onder dezelfde omstandigheden te maken hebben met gassen, kunnen we de volumeverhouding rechtstreeks gebruiken.
4. Bereken het volume van zuurstof:
Omdat de molverhouding van zuurstof tot zwaveldioxide 1:1 is, is het benodigde zuurstofvolume hetzelfde als het volume geproduceerde zwaveldioxide.
Daarom heeft u 3,5 L zuurstof nodig om te reageren met de vaste zwavel en vorm 3,5 l So₂.
Hoofdlijnen
- Wat doen de ribosomen voor cellen?
- Hoe kan onderzoekers correcte informatie verkrijgen?
- Wat is het doel van xyleem en floem?
- Wat is antimaterie en waarom doet het ertoe?
- Heeft een bacteriecel membraan?
- Wat is een fysieke verschijning genoemd door genetica?
- Wat vormt een peptidebinding?
- Waar in uw lichaam komt mitose het vaakst voor?
- Iets in de invieuring dat het gedrag van een organisme beïnvloedt, is een wat?
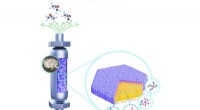
- Bindmiddelvrij titanosilicaat van het type MWW voor selectieve en duurzame epoxidatie van propyleen
- Past één maat allemaal? Een nieuw model voor organische halfgeleiders

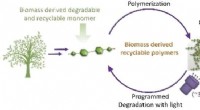
- Ontwikkelen van een degradatie-triggerbaar plastic gemaakt van vanilline
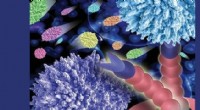
- Multisample-techniek om celadhesie te analyseren
- De lucht zuiveren:een op reductie gebaseerde oplossing voor stikstofvervuiling met een nieuwe katalysator

 Kleurenafbeeldingen herstellen van verstrooid licht
Kleurenafbeeldingen herstellen van verstrooid licht Hoe donutvormige fusieplasma's erin slaagden negatieve turbulentie te verminderen
Hoe donutvormige fusieplasma's erin slaagden negatieve turbulentie te verminderen  Is de stroom groter in elektrisch ijzer of bol?
Is de stroom groter in elektrisch ijzer of bol?  Arabische mensen hebben bijna 50 keer meer kans om te worden tegengehouden en gescand door de Britse politie
Arabische mensen hebben bijna 50 keer meer kans om te worden tegengehouden en gescand door de Britse politie Hoeveel elementen zitten er in een 2co2-atoom?
Hoeveel elementen zitten er in een 2co2-atoom?  Welke vulkanen worden gevolgd door de AVO?
Welke vulkanen worden gevolgd door de AVO?  Waar gaat de wetenschap niet over?
Waar gaat de wetenschap niet over?  Op welk punt in zijn baan heeft de komeet de grootste potentiële energie?
Op welk punt in zijn baan heeft de komeet de grootste potentiële energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


