
Wetenschap
Hoeveel liter zuurstofgas zijn aanwezig in gasgas van 11,3 gram?
1. Converteer grams naar mollen:
* De molaire massa zuurstofgas (o₂) is 32 g/mol (16 g/mol voor elk zuurstofatoom).
* Deel de massa zuurstofgas door zijn molaire massa:11,3 g / 32 g / mol =0,353 mol
2. Gebruik de ideale gaswet:
* De ideale gaswet is PV =nrt, waar:
* P =druk (we nemen standaard druk, 1 atm)
* V =volume (wat we willen vinden)
* n =aantal mol (0,353 mol)
* R =ideale gasconstante (0,0821 l · atm/mol · k)
* T =temperatuur (we nemen standaardtemperatuur, 273 K)
3. Oplossen voor volume (v):
* Herschik de ideale gaswet:V =NRT/P
* Sluit de waarden aan:V =(0,353 mol) (0,0821 L · atm / mol · k) (273 K) / (1 atm)
* Berekenen:v ≈ 8.01 l
Daarom zijn ongeveer 8,01 liter zuurstofgas aanwezig in 11,3 gram zuurstofgas bij standaardtemperatuur en druk.
 Dubbelbedkatalysator maakt een hoge omzetting van syngas in vloeibare koolwaterstoffen in het benzinebereik mogelijk
Dubbelbedkatalysator maakt een hoge omzetting van syngas in vloeibare koolwaterstoffen in het benzinebereik mogelijk Is Uranium een voorbeeld van een fossiele brandstof?
Is Uranium een voorbeeld van een fossiele brandstof?  Hoe wordt de hoeveelheid gas en zuurstof geregeld in een bunsenbrander?
Hoe wordt de hoeveelheid gas en zuurstof geregeld in een bunsenbrander?  Wat is het woordvergelijking voor cesiumchloride?
Wat is het woordvergelijking voor cesiumchloride?  Hoe wordt gas gemaakt van olie?
Hoe wordt gas gemaakt van olie?
 Welk object gebruiken milieuactivisten als een metafoor voor de aarde?
Welk object gebruiken milieuactivisten als een metafoor voor de aarde?  Wat beschrijft het zuurstofgehalte terwijl de aarde in de loop van de tijd evolueerde?
Wat beschrijft het zuurstofgehalte terwijl de aarde in de loop van de tijd evolueerde?  Enquête peilt naar de mening van topleiders over het landschap van het milieubeleid
Enquête peilt naar de mening van topleiders over het landschap van het milieubeleid NASA ontdekt dat nieuwe tropische storm Selma veel regen kan veroorzaken
NASA ontdekt dat nieuwe tropische storm Selma veel regen kan veroorzaken Klimaatvariaties kunnen invloed hebben op de basis van het voedselweb langs de kust van Californië
Klimaatvariaties kunnen invloed hebben op de basis van het voedselweb langs de kust van Californië
Hoofdlijnen
- Sommige dieren pauzeren hun eigen zwangerschappen, maar hoe ze dat doen is nog steeds een mysterie
- Het leven is mooi voor de imkers in Griekenland, maar hoe lang?
- Wat is de naam van een complex individu dat orgaansystemen bestaat?
- Een cel besteedt ongeveer hoeveel van zijn cyclus in de M -fase?
- Een opkomend tij van zeeziekten? Hoe parasieten reageren op een opwarmende wereld
- Is het Amerikaanse immigratiebeleid 'STEMming'-innovatie?
- Wat zijn de eigenschappen van een enzym?
- Produceren zaden in water zuurstof produceren?
- In welke celtypen bevinden zich ribosomen?
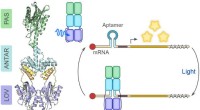
- Blauw licht voor RNA-controle
- Kleine tornado verbetert de prestaties van elektrospray-ionisatiemassaspectrometrie

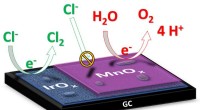
- Een stap dichter bij duurzame energie uit zeewater
- Nieuw hard-koolstofanodemateriaal voor natrium-ionbatterijen lost het lithium-raadsel op

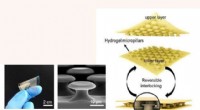
- Onderzoekers ontwikkelen nieuwe klasse onderwaterkleefstoffen
 Waarom husky’s blauwe ogen hebben
Waarom husky’s blauwe ogen hebben  Is zwavel een samengestelde element homo of heterogenus?
Is zwavel een samengestelde element homo of heterogenus?  Wat is de krachtigste waterval ter wereld?
Wat is de krachtigste waterval ter wereld?  Insecten en insecten die op kakkerlakken lijken
Insecten en insecten die op kakkerlakken lijken Studie van analoge bemanningen in isolatie onthult zwakke plekken voor Mission to Mars
Studie van analoge bemanningen in isolatie onthult zwakke plekken voor Mission to Mars Verandering van CEO vóór IPO kan waardering verhogen
Verandering van CEO vóór IPO kan waardering verhogen De meting van de concentratie waterstofionen in een oplossing wordt genoemd?
De meting van de concentratie waterstofionen in een oplossing wordt genoemd?  Om de vervuiling te verminderen, beleidsmakers moeten de focus verruimen tot verder dan schoorstenen
Om de vervuiling te verminderen, beleidsmakers moeten de focus verruimen tot verder dan schoorstenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

