
Wetenschap
Is er een chemische reactie tussen SRCL2 en COCL2?
Dit is waarom:
* Beide zijn oplosbare zouten: SRCL₂ en Cocl₂ zijn beide oplosbare ionische verbindingen. Wanneer opgelost in water, dissociëren ze in hun respectieve ionen:Sr²⁺, CL⁻, Co²⁺ en CL⁻.
* Geen drijvende kracht voor reactie: Er is geen sterke drijvende kracht om een reactie tussen deze ionen op te treden.
* Geen neerslagvorming: De potentiële producten, SRCL₂ en Cocl₂, zijn beide oplosbare zouten, dus er zou geen neerslag vormen.
* Geen gasevolutie: Er worden geen gassen gegenereerd.
* Geen significante warmteverandering: Het is onwaarschijnlijk dat de reactie zeer exotherme of endotherm is.
Samenvattend: De ionen in oplossing zullen gewoon naast elkaar bestaan als afzonderlijke entiteiten. Er is geen dwingende reden om te reageren en nieuwe verbindingen te vormen.
 Wat is het verschil tussen de twee isotopen van koper?
Wat is het verschil tussen de twee isotopen van koper?  Kunnen chemische veranderingen worden gereserveerd door fysieke veranderingen?
Kunnen chemische veranderingen worden gereserveerd door fysieke veranderingen?  Waarom is natriumchloride oplosbaar in water maar geen alcohol?
Waarom is natriumchloride oplosbaar in water maar geen alcohol?  Neutronenspectroscopie onthult dat een gewone zuurstofsponskatalysator ook waterstof opneemt
Neutronenspectroscopie onthult dat een gewone zuurstofsponskatalysator ook waterstof opneemt Onderzoekers veranderen traditioneel gif dat door Aziatische vissers wordt gebruikt voor potentiële neurologische medicijnen
Onderzoekers veranderen traditioneel gif dat door Aziatische vissers wordt gebruikt voor potentiële neurologische medicijnen
 Microplastics:geen klein probleem voor filtervoedende oceaanreuzen
Microplastics:geen klein probleem voor filtervoedende oceaanreuzen Waarom Venetië eigenlijk een schoolvoorbeeld is voor overstromingspreventie
Waarom Venetië eigenlijk een schoolvoorbeeld is voor overstromingspreventie  5.8 aardbeving rammelt Roemenië, gevoeld in Oekraïne, ergens anders
5.8 aardbeving rammelt Roemenië, gevoeld in Oekraïne, ergens anders Methaanuitstoot uit kolenmijnen hoger dan eerder gedacht
Methaanuitstoot uit kolenmijnen hoger dan eerder gedacht Slangen gevonden in Noord Illinois
Slangen gevonden in Noord Illinois
Hoofdlijnen
- Wat doet een kern in cel?
- Wat beïnvloedt de vorming van splitsingsvoren?
- Vijf olifanten gedood door trein in India
- Jackfruit uit de schappen laten springen
- Rapport:meer dan 1.000 wilde paarden naar de slachtbank gestuurd
- Het haringgenoom biedt nieuw inzicht in hoe soorten zich aanpassen aan hun omgeving
- Van groepsimmuniteit en zelfgenoegzaamheid tot groepspaniek:hoe vaccinatieangst zich ontvouwt
- Wat is wetenschappelijk woord voor recept?
- Welk proces is geen manier waarop cellen homeostase handhaven?
- Bananenplantenextract kan de sleutel zijn tot romiger, langer houdbaar ijs

- Uraniumchemie en geologische berging van radioactief afval

- Bevindingen bieden recept voor fijnafstemming van legeringen voor gebruik bij hoge temperaturen

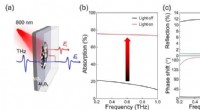
- Onderzoekers vinden breedband afstembare terahertz-absorber uit
- Ontdekking versterkt de theorie dat het leven op aarde is ontstaan uit een RNA-DNA-mix

 Welke verbinding wordt gemaakt als koper reageert met zuurstof?
Welke verbinding wordt gemaakt als koper reageert met zuurstof?  Welke drie staten van materie hebben geen eigen vorm?
Welke drie staten van materie hebben geen eigen vorm?  Wat hebben de sterren te maken met kernenergie?
Wat hebben de sterren te maken met kernenergie?  Een 2kg is druppelaar van een hoogte van 1000 m Wat de krachtluchtweerstand op obhect wanneer deze terminale snelheid racht?
Een 2kg is druppelaar van een hoogte van 1000 m Wat de krachtluchtweerstand op obhect wanneer deze terminale snelheid racht?  Waar komt het lood op natuurlijke wijze voor?
Waar komt het lood op natuurlijke wijze voor?  Waar is de zon als je een volle maan bekijkt?
Waar is de zon als je een volle maan bekijkt?  De geometrie van het leven:natuurkundigen bepalen wat de groei van biofilms controleert
De geometrie van het leven:natuurkundigen bepalen wat de groei van biofilms controleert  Welke kracht is een cadeau bij convergente grens?
Welke kracht is een cadeau bij convergente grens?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

